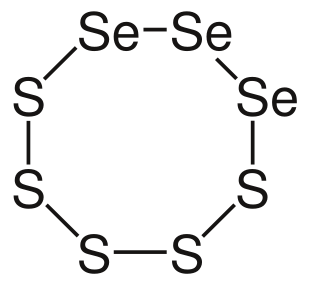
Seleendisulfide (chemische formule SeS2) is een anorganische verbinding van seleen en zwavel. Het wordt in het Nederlands vaak aangeduid als seleendisulfide of seleniumdisulfide en komt voor als een rood-oranje tot donkerrood vaste stof. SeS2 wordt gezien als een selenium(IV)-sulfide; in eenvoudige formele oxidatietoekenning staat seleen hierbij in de +4‑oxidatietoestand en zwavel als sulfide. Deze eenvoudige formulering dekt echter niet altijd de complexiteit van reële monsters, die vaak niet-stoichiometrisch en polymerisch van aard zijn. Zie ook chemische verbinding, selenium en oxidatietoestand.
Belangrijke eigenschappen
- Formule: SeS2
- Molaire massa: ongeveer 143 g·mol−1
- Uiterlijk: rood-oranje tot donkerrood vast materiaal
- Oplosbaarheid: slecht oplosbaar in water; beter oplosbaar in bepaalde organische oplosmiddelen zoals koolstofdisulfide (CS2) en vergelijkbare niet‑polarere media
- Structuur: veelal polymerisch of samengesteld uit verschillende selenium‑zwavel‑ketens; niet altijd een eenvoudig discrete molecuul
Structuur en binding
SeS2 vertoont doorgaans een complexe, deels polymerische structuur. In veel modellen is seleen gebonden aan zwavelatomen via Se–S-bindingen; daarnaast kunnen in sommige fasen ook Se–Se‑bindingen voorkomen. Daardoor zijn commerciële of synthetische monsters vaak non‑stoichiometrisch en variabel in samenstelling. De formele oxidatietoekenning waarin seleen +4 is en elk zwavelatoom −2 is, geeft een eenvoudige chemische beschrijving, maar zegt niet alles over de werkelijke, vaak gedeelde bindingen in de vaste stof.
Bereiding
- Directe samenvoeging van de elementen: verhitting van seleen met zwavel kan leiden tot vorming van SeS2, waarbij temperatuur en samenstellingsverhouding de uiteindelijke structuur en samenstelling beïnvloeden.
- Sulfidering van seleenverbindingen: reactie van seleenhalogeniden of oxide met zwavelhoudende reagentia kan ook tot selenium‑sulfiden leiden.
- Commerciële monsters zijn vaak mixtures van verschillende Se–S‑verbindingen en worden verkregen onder gecontroleerde condities om de gewenste eigenschappen te bereiken.
Reactiviteit
SeS2 kan hydrolyseren of bij sterk reducerende/oxiderende omstandigheden uiteenlopen in andere selenium‑ en zwavelverbindingen. Het reageert met sterke nucleofielen en kan bij hogere temperaturen ontleden. In organische syntheses kan het als bron van selenium of als reagens voor specifieke functiegroeptransformaties worden gebruikt, maar zijn reactiviteit en selectiviteit hangen sterk af van de feitelijke samenstelling van het gebruikte monster.
Toepassingen
- Medisch/topisch: een van de bekendste toepassingen van selenium‑sulfiden (vaak aangeduid met SeSx) is in anti‑roos en medicinale shampoos. Producten bevatten typisch lage concentraties (bijv. 1% OTC, 2,5% in sommige medicinale formuleringen) en werken antischimmel‑ en keratolytisch tegen de huidmicroflora die roos en seborrhoïsche dermatitis veroorzaakt.
- Laboratoriumreagens: gebruikt als bron van selenium in bepaalde anorganische en organische syntheses.
- Industrieel/pigmenten: op kleinere schaal toegepast vanwege de kleur en bepaalde fysisch‑chemische eigenschappen, hoewel het gebruik beperkt is door toxische en milieuoverwegingen.
Veiligheid en milieu
Seleniumverbindingen kunnen toxisch zijn voor mens en dier bij onvoldoende beheer. Seleniumsulfide in de lage concentraties die in shampoos worden gebruikt wordt over het algemeen als veilig beschouwd voor uitwendig gebruik, maar kan irritatie veroorzaken van huid en ogen en mag niet op beschadigde huid of in grote hoeveelheden worden gebruikt. Ingeslikte hoeveelheden en sterk geconcentreerde stoffen kunnen systemische toxiciteit veroorzaken. Seleniumverbindingen zijn ook schadelijk voor aquatische organismen; correcte opslag, gebruik en afvalverwerking zijn daarom belangrijk.
Analytische identificatie
De karakterisering van SeS2 gebeurt vaak met technieken als röntgendiffractie (XRD) voor vaste‑stofstructuur, Raman‑ en IR‑spectroscopie om Se–S‑ en eventuele Se–Se‑banden te identificeren, en elementaire analyse om de Se:S‑verhouding te bepalen. Omdat veel monsters niet‑stoichiometrisch zijn, is een combinatie van technieken nodig om samenstelling en structuur betrouwbaar vast te stellen.
Opmerkingen
Let op dat in de praktijk veel commerciële “selenium sulfide”-producten mengsels van selenium‑zwavelverbindingen (SeSx) zijn in plaats van een enkel zuiver SeS2-materiaal. Dit verklaart variatie in kleur, oplosbaarheid en reactiviteit tussen verschillende monsters. Bij gebruik of onderzoek is het daarom belangrijk de exacte specificatie en samenstelling van het materiaal te kennen.