Waterstofion wordt door de IUPAC aanbevolen als algemene term voor alle ionen van waterstof en de isotopen daarvan. Afhankelijk van de lading van het ion zijn er twee soorten: positief geladen ionen en negatief geladen ionen.
Waterstof ion
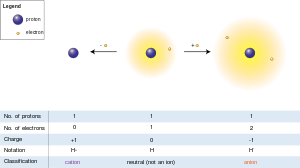

Kation (positief geladen)
Wanneer waterstof zijn elektron verliest, kunnen de kationen worden gevormd:
- Hydron: algemene naam die verwijst naar het positieve ion van een waterstofisotoop (H+ ).
- Proton: 1H+ (d.w.z. het kation van protium)
- Deuteron:2 H+ , D+
- Triton: 3H+ , T+
De ionen die ontstaan door de reactie van deze kationen met water, alsmede hun hydraten, worden ook "waterstofionen" genoemd.
In verband met zuren verwijst "waterstofionen" meestal naar hydronen.
Anion (negatief geladen)
Waterstofanionen worden gevormd wanneer extra elektronen worden verworven:
- Hydride: algemene benaming voor het negatieve ion van een waterstofisotoop (H− ).
- Protide:1 H−
- Deuteride: 2H− , D −
- Tritide:3 H− , T −