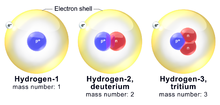
De atomen van een chemisch element kunnen voorkomen in verschillende varianten die vergelijkbaar gedrag vertonen maar verschillende massa's hebben. Deze varianten worden isotopen genoemd. Atomen van hetzelfde element hebben hetzelfde aantal protonen, maar isotopen verschillen in het aantal neutronen. Daardoor hebben isotopen een andere massa. Massa is een maat voor de hoeveelheid substantie of materie in een object; onder gelijke omstandigheden leidt dat meestal tot verschillende gewichten.
Sommige isotopen zijn onstabiel en vervallen via radioactief verval, waarbij ze veranderen in andere isotopen of in andere elementen; deze noemt men radioactieve isotopen. Andere isotopen zijn stabiel en ondergaan geen detecteerbaar radioactief verval binnen de meetbare levensduur van het systeem waarin ze voorkomen.
Het aantal protonen in een atoom bepaalt het atoomnummer en daarmee om welk element het gaat. Verschillende isotopen van een element hebben een verschillend aantal neutronen, en daardoor een ander massagetal (het aantal protonen plus neutronen). Isotopen worden doorgaans aangeduid met de naam van het element gevolgd door het massagetal, bijvoorbeeld koolstof-12 en koolstof-14, vaak geschreven als C‑12 en C‑14.
De term "isotoop" betekent letterlijk "op dezelfde plaats" en verwijst naar het feit dat isotopen van een element op dezelfde plaats in het periodiek systeem staan. Kennis over isotopen is relevant in meerdere wetenschappelijke en technologische toepassingen, zoals datering, medisch beeldvormende technieken, traceronderzoek en onderzoek naar kernenergie, waarbij eigenschappen als stabiliteit en halveringstijd van belang zijn.