Thermische fysica is, algemeen gesproken, de studie van de statistische aard van fysische systemen vanuit een energetisch perspectief. Beginnend met de grondbeginselen van warmte en temperatuur, analyseert de thermische fysica de eerste en tweede wet van de thermodynamica vanuit statistisch perspectief, in termen van het aantal microtoestanden dat overeenkomt met een bepaalde macrotoestand. Bovendien wordt het begrip entropie bestudeerd via de kwantumtheorie.
Een centraal onderwerp in de thermische fysica is de canonieke kansverdeling. De elektromagnetische aard van fotonen en fononen wordt bestudeerd, waaruit blijkt dat de oscillaties van elektromagnetische velden en van kristalroosters veel gemeen hebben. Golven vormen een basis voor beide, mits men de kwantumtheorie erbij betrekt.
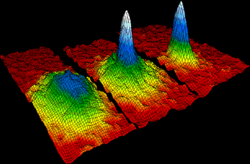
Andere onderwerpen die in de thermische fysica worden bestudeerd zijn: chemische potentiaal, het kwantumkarakter van een ideaal gas, d.w.z. in termen van fermionen en bosonen, Bose-Einstein-condensatie, vrije energie van Gibbs, vrije energie van Helmholtz, chemisch evenwicht, fase-evenwicht, het equipartitietheorema, entropie bij het absolute nulpunt, en transportprocessen als gemiddelde vrije weg, viscositeit en geleiding.