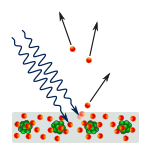
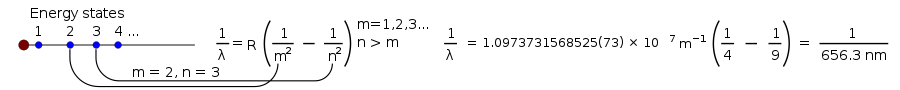De formules en ideeën van de kwantummechanica werden gemaakt om het licht te verklaren dat afkomstig is van gloeiend waterstof. De kwantumtheorie van het atoom moest ook verklaren waarom het elektron in zijn baan blijft, wat andere ideeën niet konden verklaren. Uit de oudere ideeën volgde dat het elektron in het centrum van het atoom zou moeten vallen omdat het aanvankelijk door zijn eigen energie in zijn baan wordt gehouden, maar het zou snel zijn energie verliezen wanneer het in zijn baan draait. (Dit is omdat de elektronen en andere geladen deeltjes gekend waren om licht uit te zenden en energie te verliezen wanneer zij snelheid veranderden of draaiden.)
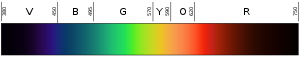
Waterstoflampen werken als neonlampen, maar neonlampen hebben hun eigen unieke groep kleuren (en frequenties) van licht. Wetenschappers ontdekten dat zij alle elementen konden identificeren aan de hand van de lichtkleuren die zij produceren. Zij konden alleen niet achterhalen hoe de frequenties werden bepaald.
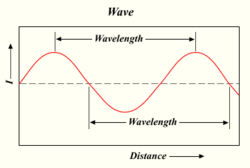
Toen bedacht de Zwitserse wiskundige Johann Balmer een vergelijking die aangaf wat λ (lambda, voor golflengte) zou zijn:
λ = B ( n 2 n 2 - 4 ) n = 3 , 4 , 5 , 6 {\displaystyle \lambda =Blink({frac {n^{2}}{n^{2}-4}}}rechts) \qquad n=3,4,5,6} 
waarbij B een getal is dat Balmer heeft vastgesteld op 364,56 nm.
Deze vergelijking werkte alleen voor het zichtbare licht van een waterstoflamp. Maar later werd de vergelijking algemener gemaakt:
1 λ = R ( 1 m 2 - 1 n 2 ) , {\displaystyle {frac {1}{lambda }}=Rleft({frac {1}{m^{2}}-{frac {1}{n^{2}}}right),}. 
waarbij R de Rydberg-constante is, gelijk aan 0,0110 nm−1 , en n groter moet zijn dan m.
Door verschillende getallen in te voeren voor m en n, kunnen gemakkelijk frequenties worden voorspeld voor vele soorten licht (ultraviolet, zichtbaar en infrarood). Om te zien hoe dit werkt, gaat u naar Hyperphysics en gaat u voorbij het midden van de pagina naar beneden. (Gebruik H = 1 voor waterstof.)
In 1908 maakte Walter Ritz het Ritz-combinatieprincipe dat laat zien hoe bepaalde hiaten tussen frequenties zich blijven herhalen. Dit bleek enkele jaren later belangrijk voor Werner Heisenberg.
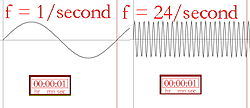
In 1905 gebruikte Albert Einstein het idee van Planck om aan te tonen dat een lichtstraal bestaat uit een stroom deeltjes die fotonen worden genoemd. De energie van elk foton hangt af van zijn frequentie. Einsteins idee is het begin van het idee in de kwantummechanica dat alle subatomaire deeltjes zoals elektronen, protonen, neutronen en andere tegelijkertijd golven en deeltjes zijn. (Zie de afbeelding van het atoom met het elektron als golven bij het atoom.) Dit leidde tot een theorie over subatomaire deeltjes en elektromagnetische golven die golf-deeltjes dualiteit wordt genoemd. Hierbij waren deeltjes en golven noch het een noch het ander, maar hadden ze bepaalde eigenschappen van beide.
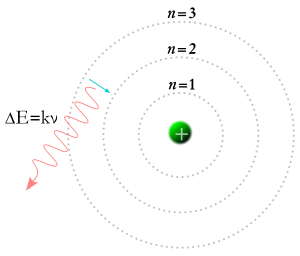
In 1913 kwam Niels Bohr met het idee dat elektronen alleen bepaalde banen rond de kern van een atoom konden aannemen. Volgens de theorie van Bohr zouden de getallen m en n in bovenstaande vergelijking banen kunnen voorstellen. Volgens de theorie van Bohr kunnen elektronen beginnen in een baan m en eindigen in een baan n, of een elektron kan beginnen in een baan n en eindigen in een baan m, dus als een foton een elektron raakt, wordt de energie ervan geabsorbeerd en gaat het elektron vanwege die extra energie naar een hogere baan. Volgens de theorie van Bohr, als een elektron van een hogere baan naar een lagere baan valt, zal het energie moeten afstaan in de vorm van een foton. De energie van het foton zal gelijk zijn aan het energieverschil tussen de twee banen, en de energie van een foton zorgt ervoor dat het een bepaalde frequentie en kleur heeft. De theorie van Bohr bood een goede verklaring voor veel aspecten van subatomaire verschijnselen, maar gaf geen antwoord op de vraag waarom elk van de kleuren licht die worden geproduceerd door gloeiend waterstof (en door gloeiend neon of een ander element) een eigen helderheid heeft, en de verschillen in helderheid altijd hetzelfde zijn voor elk element.
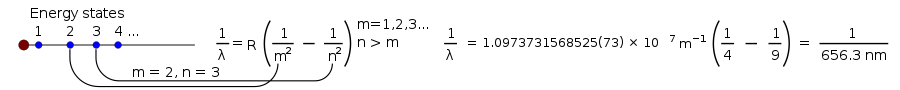
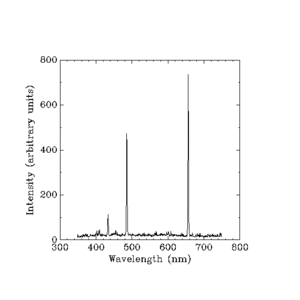
Tegen de tijd dat Niels Bohr met zijn theorie kwam, waren de meeste dingen over het door een waterstoflamp geproduceerde licht bekend, maar wetenschappers konden de helderheid van elk van de door gloeiende waterstof geproduceerde lijnen nog steeds niet verklaren.
Werner Heisenberg nam de taak op zich om de helderheid of "intensiteit" van elke lijn te verklaren. Hij kon geen eenvoudige regel gebruiken zoals die welke Balmer had bedacht. Hij moest de zeer moeilijke wiskunde van de klassieke natuurkunde gebruiken, die alles uitrekent in termen van dingen als de massa (gewicht) van een elektron, de lading (statische elektrische kracht) van een elektron, en andere kleine hoeveelheden. De klassieke natuurkunde had al antwoorden voor de helderheid van de kleurenbanden die een waterstoflamp produceert, maar de klassieke theorie zei dat er een continue regenboog moest zijn, en niet vier afzonderlijke kleurenbanden. De verklaring van Heisenberg luidt:
Er bestaat een wet die zegt welke lichtfrequenties gloeiend waterstof produceert. De wet moet uit elkaar liggende frequenties voorspellen wanneer de betrokken elektronen tussen banen dicht bij de kern (centrum) van het atoom bewegen, maar hij moet ook voorspellen dat de frequenties steeds dichter bij elkaar komen te liggen naarmate we kijken naar wat het elektron doet wanneer het verder en verder naar buiten beweegt tussen banen. Zij zal ook voorspellen dat de intensiteitsverschillen tussen de frequenties steeds dichter bij elkaar komen te liggen naarmate we verder naar buiten gaan. Waar de klassieke fysica al de juiste antwoorden geeft met één reeks vergelijkingen, moet de nieuwe fysica dezelfde antwoorden geven, maar met andere vergelijkingen.
De klassieke natuurkunde gebruikt de wiskundige methoden van Joseph Fourier om een wiskundig beeld te maken van de fysieke wereld, Het gebruikt verzamelingen gladde krommen die samengaan om één gladde kromme te maken die, in dit geval, intensiteiten geeft voor licht van alle frequenties van wat licht. Maar het klopt niet, want die gladde curve verschijnt alleen bij hogere frequenties. Bij lagere frequenties zijn er altijd geïsoleerde punten en verbindt niets de punten. Dus, om een kaart van de echte wereld te maken, moest Heisenberg een grote verandering aanbrengen. Hij moest iets doen om alleen de getallen eruit te pikken die overeenkwamen met wat men in de natuur zag. Soms zegt men dat hij deze vergelijkingen "gokte", maar hij deed geen blinde gok. Hij vond wat hij nodig had. De getallen die hij berekende zouden stippen op een grafiek zetten, maar er zou geen lijn getrokken worden tussen de stippen. En het maken van een "grafiek" van punten voor elke reeks berekeningen zou veel papier hebben verspild en niets hebben opgeleverd. Heisenberg vond een manier om de intensiteiten voor verschillende frequenties efficiënt te voorspellen en die informatie op een nuttige manier te organiseren.
Door gewoon de hierboven gegeven empirische regel te gebruiken, de regel waarmee Balmer begon en die Rydberg verbeterde, kunnen we zien hoe we een reeks getallen kunnen krijgen die Heisenberg zouden helpen het soort beeld te krijgen dat hij wilde:
De regel zegt dat wanneer het elektron van de ene baan naar de andere gaat, het energie wint of verliest, afhankelijk van de vraag of het verder van het centrum of dichterbij komt. Wij kunnen deze banen of energieniveaus dus plaatsen als kopjes langs de bovenkant en de zijkant van een rooster. Om historische redenen wordt de laagste baan n genoemd, en de volgende baan wordt n - a genoemd, dan komt n - b, enzovoort. Het is verwarrend dat men negatieve getallen gebruikte terwijl de elektronen juist energie wonnen, maar zo is het nu eenmaal.
Aangezien de Rydberg-regel ons frequenties geeft, kunnen we die regel gebruiken om getallen in te voeren, afhankelijk van waar het elektron naartoe gaat. Als het elektron begint bij n en eindigt bij n, dan is het nergens naartoe gegaan, dus heeft het geen energie gewonnen en geen energie verloren. De frequentie is dus 0. Als het elektron begint bij n-a en eindigt bij n, dan is het van een hogere baan naar een lagere baan gedaald. Dan verliest het energie, en de energie die het verliest wordt zichtbaar als een foton. Het foton heeft een bepaalde hoeveelheid energie, e, en die is gerelateerd aan een bepaalde frequentie f door de vergelijking e = h f. We weten dus dat een bepaalde verandering van baan een bepaalde lichtfrequentie, f, oplevert. Als het elektron begint bij n en eindigt bij n - a, betekent dit dat het van een lagere baan naar een hogere baan is gegaan. Dat gebeurt alleen wanneer een foton met een bepaalde frequentie en energie van buitenaf komt, door het elektron wordt geabsorbeerd en het zijn energie geeft, en dat zorgt ervoor dat het elektron naar een hogere baan gaat. Dus, om alles logisch te houden, schrijven we die frequentie als een negatief getal. Er was een foton met een bepaalde frequentie en die is nu weggenomen.
We kunnen dus een rooster als dit maken, waarbij f(a←b) de frequentie betekent die optreedt wanneer een elektron van energietoestand (baan) b naar energietoestand a gaat (Nogmaals, de reeksen zien er achterstevoren uit, maar zo werden ze oorspronkelijk geschreven):
Raster van f
| Elektronenstaten | n | n-a | n-b | n-c | .... | |
| n | f(n←n) | f(n←n-a) | f(n←n-b) | f(n←n-c) | ..... | |
| n-a | f(n-a←n) | f(n-a←n-a) | f(n-a←n-b) | f(n-a←n-c) | ..... | |
| n-b | f(n-b←n) | f(n-b←n-a) | f(n-b←n-b) | f(n-b←n-c) | ..... | |
| transitie.... | ..... | ..... | ..... | ..... | | |
Heisenberg heeft de roosters niet zo gemaakt. Hij deed alleen de wiskunde waarmee hij de intensiteiten kreeg die hij zocht. Maar daarvoor moest hij twee amplitudes (de hoogte van een golf) met elkaar vermenigvuldigen om de intensiteit te berekenen. (In de klassieke natuurkunde is intensiteit gelijk aan amplitude in het kwadraat.) Hij maakte een vreemde vergelijking om dit probleem op te lossen, schreef de rest van zijn artikel uit, overhandigde het aan zijn baas en ging op vakantie. Dr. Born keek naar zijn grappige vergelijking en het leek een beetje gek. Hij moet zich hebben afgevraagd: "Waarom heeft Heisenberg mij dit rare ding gegeven? Waarom moet hij het zo doen?" Toen realiseerde hij zich dat hij keek naar een blauwdruk voor iets dat hij al heel goed kende. Hij was gewend om het rooster of de tabel die we konden schrijven door bijvoorbeeld alle wiskunde voor frequenties te doen, een matrix te noemen. En de vreemde vergelijking van Heisenberg was een regel om twee van die matrices met elkaar te vermenigvuldigen. Max Born was een zeer, zeer goede wiskundige. Hij wist dat, aangezien de twee matrices (rasters) die met elkaar werden vermenigvuldigd verschillende dingen vertegenwoordigden (zoals positie (x,y,z) en momentum (mv), bijvoorbeeld), je bij vermenigvuldiging van de eerste matrix met de tweede een antwoord kreeg en bij vermenigvuldiging van de tweede matrix met de eerste matrix een ander antwoord. Ook al had hij geen verstand van matrixwiskunde, Heisenberg zag dit "verschillende antwoorden" probleem al en hij had er last van. Maar Dr. Born was zo'n goede wiskundige dat hij zag dat het verschil tussen de eerste matrixvermenigvuldiging en de tweede matrixvermenigvuldiging altijd te maken had met de constante van Planck, h, vermenigvuldigd met de vierkantswortel van negatief één, i. Dus binnen een paar dagen na Heisenbergs ontdekking hadden ze al de basiswiskunde voor wat Heisenberg graag het "onbepaaldheidsprincipe" noemde. Met "onbepaaldheid" bedoelde Heisenberg dat iets als een elektron niet vastligt totdat het vastligt. Het is een beetje als een kwal die altijd rondkruipt en niet "op één plaats" kan zijn tenzij je hem doodt. Later kregen mensen de gewoonte om het "Heisenbergs onzekerheidsprincipe" te noemen, waardoor veel mensen de fout maakten te denken dat elektronen en dat soort dingen echt "ergens" zijn, maar dat we er alleen in ons eigen hoofd onzeker over zijn. Dat idee is verkeerd. Het is niet waar Heisenberg het over had. Moeite hebben met het meten van iets is een probleem, maar het is niet het probleem waar Heisenberg het over had.
Heisenbergs idee is erg moeilijk te begrijpen, maar we kunnen het duidelijker maken met een voorbeeld. Eerst zullen we deze rasters "matrices" gaan noemen, omdat we het straks over matrixvermenigvuldiging moeten hebben.
Stel dat we beginnen met twee soorten metingen, positie (q) en momentum (p). In 1925 schreef Heisenberg een vergelijking als deze:
Y ( n , n - b ) = ∑ a p ( n , n - a ) q ( n - a , n - b ) {\displaystyle Y(n,n-b)=sum _{a}^{},p(n,n-a)q(n-a,n-b)} (Vergelijking voor de geconjugeerde variabelen impuls en positie)
(Vergelijking voor de geconjugeerde variabelen impuls en positie)
Hij wist het niet, maar deze vergelijking geeft een blauwdruk voor het uitschrijven van twee matrices (roosters) en het vermenigvuldigen ervan. De regels voor het vermenigvuldigen van de ene matrix met de andere zijn een beetje rommelig, maar hier zijn de twee matrices volgens de blauwdruk, en dan hun product:
Matrix van p
| Elektronenstaten | n-a | n-b | n-c | .... | |
| n | p(n←n-a) | p(n←n-b) | p(n←n-c) | ..... | |
| n-a | p(n-a←n-a) | p(n-a←n-b) | p(n-a←n-c) | ..... | |
| n-b | p(n-b←n-a) | p(n-b←n-b) | p(n-b←n-c) | ..... | |
| transitie.... | ..... | ..... | ..... | ..... | |
Matrix van q
| Elektronenstaten | n-b | n-c | n-d | .... | |
| n-a | q(n-a←n-b) | q(n-a←n-c) | q(n-a←n-d) | ..... | |
| n-b | q(n-b←n-b) | q(n-b←n-c) | q(n-b←n-d) | ..... | |
| n-c | q(n-c←n-b) | q(n-c←n-c) | q(n-c←n-d) | ..... | |
| transitie.... | ..... | ..... | ..... | ..... | |
De matrix voor het product van de bovenstaande twee matrices zoals gespecificeerd door de relevante vergelijking in Heisenberg's 1925 paper is:
| Elektronenstaten | n-b | n-c | n-d | ..... |
| n | A | ..... | ..... | ..... |
| n-a | ..... | B | ..... | ..... |
| n-b | ..... | ..... | C | ..... |
Waar:
A=p(n←n-a)*q(n-a←n-b)+p(n←n-b)*q(n-b←n-b)+p(n←n-c)*q(n-c←n-b)+.....
B=p(n-a←n-a)*q(n-a←n-c)+p(n-a←n-b)*q(n-b←n-c)+p(n-a←n-c)*q(n-c←n-c)+.....
C=p(n-b←n-a)*q(n-a←n-d)+p(n-b←n-b)*q(n-b←n-d)+p(n-b←n-c)*q(n-d←n-d)+.....
enzovoort.
Als de matrices zouden worden omgekeerd, zou dit de volgende waarden opleveren:
A=q(n←n-a)*p(n-a←n-b)+q(n←n-b)*p(n-b←n-b)+q(n←n-c)*p(n-c←n-b)+.....
B=q(n-a←n-a)*p(n-a←n-c)+q(n-a←n-b)*p(n-b←n-c)+q(n-a←n-c)*p(n-c←n-c)+.....
C=q(n-b←n-a)*p(n-a←n-d)+q(n-b←n-b)*p(n-b←n-d)+q(n-b←n-c)*p(n-d←n-d)+.....
enzovoort.
Merk op hoe het veranderen van de volgorde van vermenigvuldiging stap voor stap de getallen verandert die daadwerkelijk worden vermenigvuldigd.