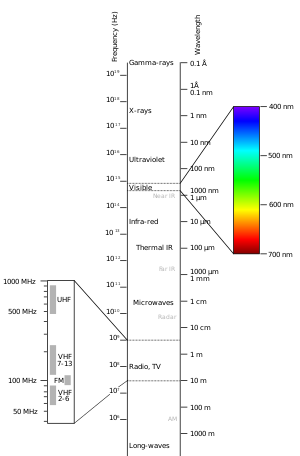
UV-zichtbare absorptie is het proces waarbij een molecuul ultraviolet of zichtbaar licht opneemt zodat elektronen naar een hogere energietoestand worden gebracht. Die opname verhoogt de energie van het systeem en veroorzaakt een overgang van de grondtoestand naar één of meer aangeslagen toestanden. Dit fenomeen vormt de basis van de analytische techniek absorptiespectroscopie, meer specifiek van wat men UV‑vis spectroscopie noemt.
Basisprincipes
In UV‑vis spectroscopie wordt licht door een oplossing of vaste stof gestuurd en wordt gemeten welke golflengten worden geabsorbeerd. Een absorptiespectrum toont de absorptie (of optische dichtheid) als functie van golflengte. Typische grootheden zijn:
- λmax — de golflengte waarop de absorptie maximaal is.
- ε (molaire extinctiecoëfficiënt) — maat voor hoe sterk een stof licht absorbeert bij een bepaalde golflengte.
- A — de geobserveerde absorptie (optische dichtheid).
Elektronische overgangen
Verschillende typen elektronische overgangen veroorzaken absorptie in verschillende delen van het spectrum:
- π → π* : komen typisch voor bij geconjugeerde dubbele bindingen en geven vaak sterke absorptie in het UV/vis-gebied.
- n → π* : optreden bij niet‑gebonden elektronen (zoals bij carbonylgroepen); deze overgangen zijn vaak zwakker en kunnen naar langere golflengten verschuiven.
- σ → σ* : vereisen meestal veel energie en treden op in de diepe UV.
De aanwezigheid van conjugatie, ringstructuren en elektronische substituenten beïnvloedt zowel de positie van λmax als de intensiteit (ε).
Instrumentatie en werking
Een UV‑vis-spectrometer bestaat grofweg uit:
- Een lichtbron (bijv. deuteriumlamp voor UV en halogeenlamp voor zichtbaar).
- Een monochromator of een grating om specifieke golflengten te selecteren (of een polychromator in een fotodiode-array detector).
- Een cuvet of monsterkamer (voor UV vaak kwarts cuvetten gebruiken omdat glas UV absorbeert).
- Een detector (bijv. fotomultiplicator of fotodiode-array) die de intensiteit meet.
Spectrumopnames kunnen in één punt (fixed‑wavelength), als scans over een bereik, of in realtime met snelle detectors uitgevoerd worden.
Kwantificering: de Wet van Beer‑Lambert
Voor kwantitatieve analyse gebruikt men de Wet van Beer‑Lambert:
A = ε · l · c
- A = absorptie (adimensioneel)
- ε = molaire extinctiecoëfficiënt (L·mol⁻¹·cm⁻¹)
- l = padlengte van de cuvet (cm)
- c = concentratie van de absorberende soort (mol·L⁻¹)
De wet geldt onder ideale omstandigheden (niet te hoge concentraties, geen verstoring door nevenreacties of turbiditeit). Kalibratielijnen met standaarden verbeteren de nauwkeurigheid.
Monstervoorbereiding en praktische tips
- Kies een oplosmiddel dat zelf niet absorbeert bij de te meten golflengte (bijv. acetonitril of methanol voor veel organische verbindingen; voor diepe UV: kwarts en geschikte oplosmiddelen).
- Gebruik geschikte cuvetten: kwarts voor UV, optisch glas of kunststof voor zichtbaar als de golflengtes dat toelaten.
- Werk binnen het lineaire bereik van de Beer‑Lambert wet: vaak A tussen ~0,1 en 1,0. Verdun monsters die te sterk absorberen.
- Controleer en corrigeer voor achtergrondabsorptie (blanco met oplosmiddel) en baseline‑drift.
Toepassingen
UV‑vis spectroscopie is breed inzetbaar:
- Kwantiatieve analyse — bepaling van concentraties van chromofore stoffen in oplossing.
- Kwalitatieve identificatie — vergelijken van λmax en bandprofielen voor structurele informatie.
- Kinetiek — volgen van reacties in de tijd door verandering in absorptie bij specifieke golflengten.
- Zuiverheidscontrole — detectie van onzuiverheden of degradeerproducten.
- Milieu- en farmaceutische analyses — bepaling van verontreinigingen en formuleringen.
Beperkingen
UV‑vis spectroscopie is niet altijd selectief: verschillende stoffen kunnen op vergelijkbare golflengten absorberen. Bovendien geeft de techniek vooral informatie over elektronische structuur, maar weinig directe detail over exacte molecuulstructuur (waarvoor IR, NMR of MS nuttig zijn). Blumige of deeltjeshoudende monsters kunnen verstoringen veroorzaken doordat ze licht verstrooien in plaats van absorberen.
Samenvattend: UV‑vis absorptie is een eenvoudige, snelle en veelgebruikte techniek om elektronische overgangen in moleculen te bestuderen en concentraties te bepalen. Goede monster‑ en oplosmiddelselectie, juiste instrumentinstellingen en begrip van de onderliggende overgangen verhogen de betrouwbaarheid van de resultaten.