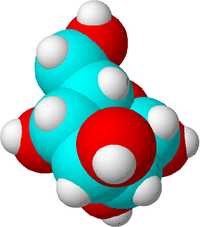
Een molecuul is de kleinste hoeveelheid van een chemische stof die kan bestaan. Als een molecuul in kleinere stukken zou worden gesplitst, zou het een andere stof zijn.
Moleculen bestaan uit atomen die in een bepaalde vorm aan elkaar zijn geplakt. Niet alle combinaties van atomen zijn even goed mogelijk; atomen maken bepaalde vormen bij voorkeur boven andere. Ook hebben ze een andere valentie. Zo hebben zuurstofatomen altijd twee bindingen met andere atomen, koolstofatomen hebben altijd vier bindingen met andere atomen en stikstofatomen hebben altijd drie bindingen met andere atomen.
In de kinetische theorie van gassen wordt de term molecuul vaak gebruikt voor elk gasvormig deeltje, ongeacht de samenstelling ervan. Volgens deze definitie worden edelgasatomen beschouwd als moleculen, omdat het in feite monoatomaire moleculen zijn.
In gassen zoals lucht vliegen de moleculen gewoon rond. In vloeistoffen zoals water zitten de moleculen aan elkaar vast, maar ze kunnen nog steeds bewegen. In vaste stoffen zoals suiker kunnen de moleculen alleen maar vibreren. In de vierde toestand van materie die bekend staat als plasma, zijn de atomen geïoniseerd en kunnen ze geen moleculen vormen.
Met een moleculaire formule kun je de aantallen van alle atomen in een molecuul opschrijven. De moleculaire formule van glucose is bijvoorbeeld C6H12O6. Dat betekent dat één molecuul glucose bestaat uit zes koolstofatomen, twaalf waterstofatomen en zes zuurstofatomen.