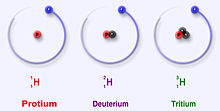
Waterstof heeft drie belangrijke isotopen: protium (1H), deuterium (2H) en tritium (3H). Deze isotopen komen van nature voor in de natuur. Protium en deuterium zijn stabiel. Tritium is radioactief en heeft een halveringstijd van ongeveer 12 jaar. Wetenschappers hebben nog vier andere waterstofisotopen (4H tot 7H) gemaakt, maar deze isotopen zijn zeer instabiel en bestaan niet in de natuur.
De belangrijkste isotopen van waterstof zijn uniek omdat zij de enige isotopen zijn die een naam hebben. Deze namen zijn nog steeds in gebruik. Deuterium en tritium krijgen soms hun eigen symbolen, D en T. De Internationale Unie voor Zuivere en Toegepaste Scheikunde is echter niet erg gecharmeerd van deze namen, ook al worden ze vaak gebruikt. Er zijn nog andere isotopen die hun eigen naam hadden toen wetenschappers radioactiviteit bestudeerden. Maar hun namen worden vandaag niet meer gebruikt.