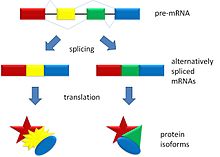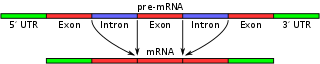
Alternatieve splitsing maakt het mogelijk dat één stukje DNA kan leiden tot meerdere verschillende eiwitten. Door variatie in de exon-samenstelling van het eindige boodschapper RNA (mRNA) ontstaan verschillende mRNA‑isoformen die uit hetzelfde gen worden afgelezen.
Wat is alternatieve splicing?
Bij alternatieve splicing worden de exons van het pre-messenger RNA, geproduceerd door transcriptie, op verschillende manieren samengevoegd tijdens de RNA-splicing. Het resultaat is dat één gen meerdere verschillende rijpe boodschapper‑RNA's kan produceren. Deze mRNA‑isoformen worden vervolgens vertaald in verschillende eiwitten (of soms niet vertaald als ze worden afgebroken), waardoor de functionele diversiteit van het eiwitbestand (proteoom) toeneemt. Bij de mens ondergaat ongeveer 95% van de multiexonische genen alternatieve splicing.
Mechanisme en betrokken factoren
De kern van splicing wordt gevormd door het spliceosoom, een groot complex van kleine nucleaire RNA's en eiwitten (snRNPs). Dit complex herkent kernsequenties in het pre-mRNA, zoals het 5'-splice site, het 3'-splice site en de branch point-plaats, en knipt en plakt introns er tussenuit.
Kernbegrippen:
- Cis‑elementen: korte sequenties in het pre-mRNA (splice sites, branch point, polypyrimidine tract, exonic/intronic splicing enhancers of silencers).
- Trans‑factoren: eiwitten die binden aan de cis‑elementen en splicing bevorderen of remmen. Voorbeelden zijn SR‑proteïnen (activatoren) en hnRNP's (vaak repressoren).
Door de combinatie van deze signalen kan hetzelfde pre-mRNA in verschillende cellen, ontwikkelingsstadia of condities anders worden gespleten.
Belangrijke typen alternatieve splicing
Er bestaan meerdere manieren waarop exons en introns kunnen variëren:
- Exon skipping (cassette exon): een exon wordt in sommige isoformen weggelaten.
- Meestal wederzijds exclusieve exons: twee exons worden nooit samen opgenomen; slechts één van beide verschijnt in het rijpe mRNA.
- Alternatieve 5'- of 3'-splice sites: gebruik van een ander begin- of eindpunt van een exon leidt tot verkorting of verlenging van dat exon.
- Intronretentie: een intron wordt niet verwijderd en blijft in het uiteindelijke mRNA aanwezig.
Functionele gevolgen
Alternatieve splicing kan leiden tot eiwitten met verschillende eigenschappen: veranderde bindingsdomeinen, subcellulaire lokalisatie, enzymatische activiteit of afbraakgevoeligheid. Sommige splicing‑varianten introduceren een vroeg stopcodon; zulke transcripten worden vaak herkend door het nonsense‑mediated decay (NMD) Splicing wordt niet alleen bepaald door de sequência's in het RNA, maar ook door factoren zoals: Abnormale splicing kan ziekte veroorzaken of eraan bijdragen. Voorbeelden en mechanismen: Therapeutische strategieën die splicing beïnvloeden omvatten: Moderne methoden om alternatieve splicing te bestuderen: Alternatieve splicing is een krachtige en wijdverspreide manier om de diversiteit van eiwitten uit één gen te vergroten. Het wordt gereguleerd door een samenspel van cis‑elementen en trans‑factoren, is cruciaal voor normale ontwikkeling en weefselfunctie, en speelt een belangrijke rol bij tal van ziektes. Dankzij diepgaande kennis van de mechanismen van splicing zijn er inmiddels gerichte therapieën ontstaan die splicing selectief kunnen aanpassen. Niet‑werkende of foutieve splicing producten worden in cellen vaak behandeld door post‑transcriptionele kwaliteitscontrole; dat wil zeggen dat ze worden herkend en versneden of afgebroken door gespecialiseerde enzymen en kwaliteitscontrolemechanismen.Regulatie en context
Alternatieve splicing bij ziekte en therapeutische benaderingen
Detectie en onderzoek
Samenvatting