Enzymen zijn eiwitmoleculen in cellen die werken als biologische katalysatoren. Enzymen versnellen chemische reacties in het lichaam, maar raken daarbij niet uitgeput en kunnen dus steeds weer opnieuw worden gebruikt.
Voor bijna alle biochemische reacties in levende wezens zijn enzymen nodig. Met een enzym verlopen chemische reacties veel sneller dan zonder het enzym het geval zou zijn. p39 Andere biokatalysatoren zijn katalytische RNA-moleculen, ribozymen genoemd.
De stoffen aan het begin van een reactie worden substraten genoemd. De stoffen aan het eind van een reactie zijn de producten. Enzymen werken op de substraten en maken er producten van. De studie van enzymen wordt enzymologie genoemd.
Het eerste enzym werd in 1833 gevonden door Anselme Payen.
Hoe werken enzymen?
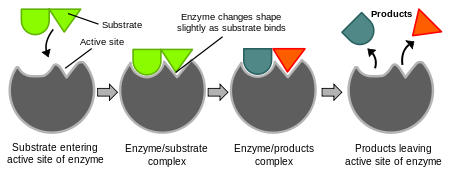
Enzymen verlagen de activeringsenergie van een reactie, zodat reacties bij lagere temperatuur en sneller kunnen verlopen. Belangrijk in die werking is het actieve centrum, een kleine regio van het enzym waarin het substraat bindt. Door de specifieke vorm en chemische eigenschappen van het actieve centrum past een bepaald substraat vaak precies, waardoor grote specificiteit ontstaat.
Twee veelgebruikte modellen om binding te beschrijven zijn:
- Lock-and-key: het actieve centrum en het substraat passen als sleutel en slot.
- Induced fit: het enzym verandert licht van vorm bij binding, waardoor substraten nog beter gepositioneerd worden voor de reactie.
Factoren die enzymactiviteit beïnvloeden
Enzymactiviteit hangt af van verschillende omgevings- en moleculaire factoren:
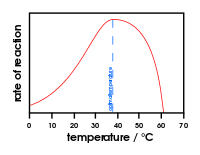
- Temperatuur: bij toenemende temperatuur neemt de reactiesnelheid vaak toe tot een optimum; daarboven denatureert het eiwit en valt activiteit weg.
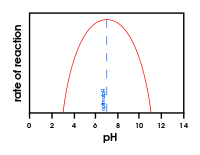
- pH: elk enzym heeft een optimaal pH-bereik; afwijkingen beïnvloeden ladingen in het actieve centrum en verminderen activiteit.
- Substraatconcentratie: bij lage concentratie stijgt de reactiesnelheid met meer substraat, tot de enzymen verzadigd raken (Vmax).
- Remmers (inhibitors): competitieve remmers binden in het actieve centrum, niet-competitieve remmers verminderen de activiteit door elders te binden; sommige remmers zijn irreversibel.
- Cofactoren en co-enzymen: veel enzymen hebben metalen ionen (bijv. Mg2+, Zn2+) of organische cofactoren (bijv. NAD+, vitamine-afgeleiden) nodig om te functioneren.
Kinetiek en begrippen
Enzymkinetiek beschrijft hoe snel enzymreacties verlopen. De Michaelis–Menten-vergelijking is een veelgebruikt model met twee belangrijke grootheden:
- Km — de Michaelis-constante: een maat voor de affiniteit van het enzym voor het substraat (laag Km = hoge affiniteit).
- Vmax — maximale reactiesnelheid bij verzadiging.
Een ander belangrijk begrip is kcat (turnover number): het aantal substraatmoleculen dat één enzymmolecuul per seconde omzet onder optimale omstandigheden.
Classificatie en soorten enzymen
Enzymen worden doorgaans ingedeeld in zes hoofdklassen volgens de EC-classificatie:
- Oxidoreductasen (redoxreacties)
- Transferasen (groepenoverdracht)
- Hydrolasen (hydrolyse)
- Lyasen (groep-eliminaties)
- Isomerasen (isomerisaties)
- Ligases (vorming van bindingen, vaak ATP-verbruik)
Voorbeelden: amylase (hydrolase) breekt zetmeel af; DNA-polymerase is een ligase-achtige activiteit bij DNA-synthese; ATP-synthase vormt ATP.
Regulatie van enzymen
Enzymen worden nauwkeurig gereguleerd zodat cellen reageren op veranderende behoeften:
- Allosterische regulatie: binding van effectoren op een andere plaats dan het actieve centrum verandert de activiteit.
- Covalente modificatie: bijvoorbeeld fosforylering/de-fosforylering schakelt enzymen aan of uit.
- Veranderingen in expressie: cellen maken meer of minder van een enzym via genregulatie.
Biologische en medische betekenis
Enzymen zijn essentieel voor stofwisseling, energieproductie, DNA-replicatie, signaaltransductie en nog veel meer. Klinisch en praktisch belangrijke punten:
- Enzymdeficiënties kunnen erfelijke ziektes veroorzaken (bijv. fenylketonurie door gebrek aan fenylalaninehydroxylase).
- Enzymen als biomarkers: verhoogde waarden van leverenzymen (ALT, AST) of hartenzymen (troponine, CK-MB) worden gebruikt bij diagnose van orgaanschade.
- Geneesmiddelen kunnen enzymen remmen of activeren (bijv. ACE-remmers, HIV-proteaseremmers).
- Toepassingen in industrie en geneeskunde: enzymen worden gebruikt in wasmiddelen, voedselproductie (b.v. kaas, bier), biotechnologie (PCR, sequencing) en therapeutische enzymen (bloedstolsel-oplossende middelen).
Samenvatting
Enzymen zijn gespecialiseerde eiwitten die bijna alle biochemische reacties in levende organismen mogelijk en efficiënt maken. Ze werken via een actief centrum dat substraten herkent en omzet, en hun activiteit wordt beïnvloed door temperatuur, pH, concentraties, cofactors en regulatoire mechanismen. Kennis over enzymen is essentieel voor biochemie, geneeskunde en vele toepassingen in de industrie.