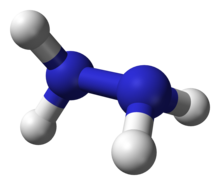
Hydrazine, ook bekend als diazine, is een chemische verbinding. Het bestaat uit stikstof- en waterstofionen. De chemische formule is N2H4. Het bevat waterstof in de +1 en stikstof in de -2 oxidatietoestand.
Wat is hydrazine?
Hydrazine (structuur H2N–NH2) is een kleurloze, olieachtige vloeistof met een scherpe, ammoniakachtige geur. Het is goed oplosbaar in water en in veel polaire organische oplosmiddelen. In de handel wordt hydrazine vaak als hydrazine-hydraat (N2H4·H2O) geleverd.
Belangrijke eigenschappen
- Fysische eigenschappen: vrij laag smeltpunt (ongeveer 2 °C) en kookpunt rond 114 °C; mengbaar met water.
- Chemische eigenschappen: een sterke reductie-middel; basisch in waterige oplossing (vormt het hydrazinium-ion N2H5+); kan makkelijk geoxideerd of ontleed worden tot stikstof en waterstof.
- Reactiviteit: reageert heftig met oxiderende middelen en kan met bepaalde metalen en metalen zouten onstabiele of explosieve mengsels vormen.
Productie en industriële bereiding
Industriële productie van hydrazine gebeurt meestal via processen waarin ammoniak wordt omgezet met behulp van oxiderende reagentia en een geschikte koolstofdrager (bijvoorbeeld ketonen). Een vaak toegepaste methode is het zogenaamde keton- of peroxideproces: hierbij reageert ammoniak met waterstofperoxide in aanwezigheid van een keton (bijvoorbeeld acetone) waardoor tijdelijk azines ontstaan die vervolgens worden gehydrolyseerd tot hydrazine; de keton kan worden teruggewonnen en hergebruikt. Historisch bestaan er meerdere processen (Raschig-type, Bayer-processen), maar moderne installaties zetten vooral peroxide-gebaseerde routes in vanwege hogere selectiviteit en minder bijproducten.
Toepassingen
- Raketbrandstof en monopropellanten: hydrazine en bepaalde derivaten (zoals monomethylhydrazine en dimethylhydrazine) worden gebruikt als hypergolische brandstoffen en als monopropellant in stuwraketten en thrusters voor satellieten vanwege hun hoge energiedichtheid en betrouwbare ontstekingseigenschappen.
- Waterbehandeling: hydrazine werkt als zuurstofscavenger in stoomketels en industriële watersystemen; het reduceert opgelost zuurstof en voorkomt corrosie van metalen leidingen en ketels.
- Organische synthese: gebruikt als reductor en tussenproduct bij de bereiding van farmaca, agrochemicaliën, kleurstoffen en schuimmiddelen; veel synthetische routes maken gebruik van hydrazine of zijn derivaten.
- Polymerisatie-initiatie en schuimmiddelen: sommige toepassingen in polymeren en schuimproductie gebruiken hydrazine-verbindingen als blazend of als initiator.
- Energie- en brandstofcellen: hydrazine wordt onderzocht en soms toegepast in speciale brandstofcellen en als energie-drager in nichetoepassingen.
Gezondheid, veiligheid en milieu
Gevaarlijkheid: hydrazine is zeer toxisch bij inademing, opname of opname via de huid. Kortdurende blootstelling kan irritatie van ogen, neus en keel veroorzaken; hogere of langdurige blootstelling kan schade geven aan lever, nieren en centraal zenuwstelsel. Hydrazine wordt beschouwd als vermoedelijk kankerverwekkend en er gelden strikte blootstellingslimieten in de industrie.
Brand- en explosiegevaar: hydrazine is brandbaar en kan in mengsels met lucht ontploffingsgevaarlijk zijn. Het reageert heftig met sterke oxidatoren. Gebruik geen open vuur of vonken in de nabijheid.
Milieu: hydrazine is zeer toxisch voor aquatische organismen; lozing in het milieu moet worden vermeden. Het breekt onder bepaalde omstandigheden af tot minder schadelijke producten, maar gevaar voor acute ecotoxiciteit blijft bestaan.
Opslag en omgang
- Bewaar hydrazine in goed afgesloten, gecertificeerde containers, bij voorkeur onder inert gas en op een koele, goed geventileerde plaats.
- Vermijd contact met oxidatoren, halogenen en zware metalen of hun zouten.
- Gebruik passende persoonlijke beschermingsmiddelen: chemisch-bestendige handschoenen, veiligheidsbril, gezichtsscherm en, bij risico op inhalatie, geschikte ademhalingsbescherming.
- Bij morsen: uitgifte beperken, kleine hoeveelheden neutraliseren volgens bedrijfsprocedures en afval laten verwerken door bevoegde diensten.
Detectie en analyse
Hydrazine kan worden gedetecteerd en gekwantificeerd met diverse analytische methoden, zoals gaschromatografie (GC) na derivatisering, HPLC, spectrofotometrische methoden (bijvoorbeeld reactie met p-dimethylaminobenzaldehyde) en elektrochemische sensoren. Regelmatige monitoren van lucht en proceswater is belangrijk in omgevingen waar hydrazine wordt gebruikt.
Alternatieven en regelgeving
Vanwege de hoge toxiciteit en milieuproblemen wordt in sommige toepassingen gezocht naar alternatieven (minder giftige zuurstofscavengers, andere brandstofoptions voor stuwsystemen, of groene reductiemethoden). Hydrazinegebruik is onderworpen aan strenge veiligheidsregels en milieuvoorschriften; bedrijven moeten voldoen aan arbeidsveiligheids- en chemikaliënbesluitgeving en de juiste risicobeoordelingen en vergunningen hebben.
Belangrijk: bij twijfel of bij incidenten altijd de veiligheidsinformatiebladen (SDS) raadplegen en de procedures van uw organisatie volgen. Hydrazine is een gevaarlijke stof — professionele training en strikte veiligheidsmaatregelen zijn noodzakelijk bij werkzaamheid ermee.