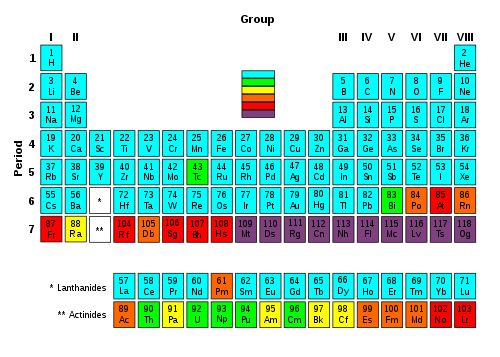
De chemische elementen buiten lood zijn radioactief, en ze hebben geen stabiele isotopen. Dit betekent dat ze zullen vervallen in andere elementen. Behalve Plutonium, is hun halfwaardetijd in de orde van enkele minuten, tot seconden. Er is een theorie in de natuurkunde die zegt dat er na een aantal elementen met een korte halfwaardetijd, andere met een langere halfwaardetijd zullen zijn. Deze staan algemeen bekend als Eilanden van Stabiliteit. Van deze elementen wordt verwacht dat ze isotopen hebben met een halfwaardetijd in de orde van enkele minuten. De hypothese is dat de atoomkern is opgebouwd in "shells" op een manier die vergelijkbaar is met de structuur van de veel grotere elektronenschelpen in atomen. In beide gevallen zijn schelpen slechts groepen van quantumenergieniveaus die relatief dicht bij elkaar liggen. Energieniveaus van kwantumtoestanden in twee verschillende schelpen worden gescheiden door een relatief groot energieverschil. Dus als het aantal neutronen en protonen de energieniveaus van een bepaalde schelp in de kern volledig vult, zal de bindingsenergie per kern een lokaal maximum bereiken en dus zal die bepaalde configuratie een langere levensduur hebben dan de nabijgelegen isotopen die geen gevulde schelpen bezitten.
Een gevulde schelp zou "magische getallen" van neutronen en protonen hebben. Een mogelijk magisch aantal neutronen voor sferische kernen is 184, en enkele mogelijke overeenkomende protonnummers zijn 114, 120 en 126 - wat zou betekenen dat de meest stabiele sferische isotopen Flerovium-298, unbinilium-304 en unbihexium-310 zouden zijn. Van bijzonder belang is Ubh-310, wat "dubbel magisch" zou zijn (zowel het protonnummer van 126 als het neutronnummer van 184 worden verondersteld magisch te zijn) en dus het meest waarschijnlijk een zeer lange halfwaardetijd te hebben. (De volgende lichtere dubbele magische bolkern is lood-208, de zwaarste stabiele kern en het meest stabiele zware metaal).
Recent onderzoek geeft aan dat grote kernen vervormd zijn, waardoor er magische getallen verschuiven. Hassium-270 wordt nu verondersteld een dubbele magische vervormde kern te zijn, met vervormde magische getallen 108 en 162. Het heeft echter een halfwaardetijd van slechts 3,6 seconden.
Isotopen zijn geproduceerd met genoeg protonen om ze op een stabiel eiland te planten, maar met te weinig neutronen om ze zelfs op de buitenste "oevers" van het eiland te plaatsen. Het is mogelijk dat deze elementen ongewone chemische eigenschappen hebben en, als ze isotopen hebben met een adequate levensduur, beschikbaar zouden zijn voor verschillende praktische toepassingen (zoals deeltjesversnellerdoelen en ook als neutronenbron).