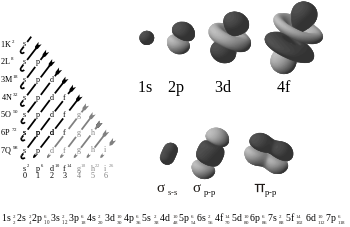
In de chemie zijn pi-bindingen (π-bindingen) covalente chemische bindingen waarbij het orbitale pad van het ene elektron kruist (overlapt) met het pad van een ander elektron. De elektronen hebben een kwabvormig figuur van acht banen (zie afbeelding). Er zijn twee overlappingsgebieden omdat de banen elkaar op beide lobben overlappen. Slechts één van de knooppuntvlakken van de baan gaat door beide betrokken kernen.
De Griekse letter π in hun naam verwijst naar p orbitalen. De orbitale symmetrie van de pi-binding ziet er hetzelfde uit als die van de p-binding als je naar beneden kijkt. P-banen hebben meestal een dergelijke binding. D-banen worden ook verondersteld pi-binding te gebruiken, maar dit is niet noodzakelijkerwijs wat er in de werkelijkheid gebeurt. Het idee van binding van d-banen past in de theorie van de hypervalentie.
Pi-bindingen zijn meestal zwakker dan sigma-bindingen. Quantummechanica zegt dat dit komt omdat de orbitale paden parallel lopen zodat er veel minder overlap is tussen de p-orbitalen.
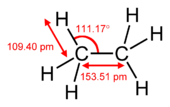
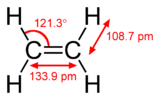
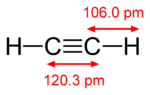
Pi-bindingen ontstaan wanneer twee atoombanen met elkaar in contact komen door twee overlappende gebieden. Pi-bindingen zijn meer gespreide bindingen dan de sigma-bindingen. Elektronen in pi-bindingen worden soms pi elektronen genoemd. Moleculaire fragmenten die met elkaar verbonden zijn door een pi-binding kunnen niet om die binding heen draaien zonder de pi-binding te verbreken. De rotatie vernietigt de parallelle paden van de twee p-banen.