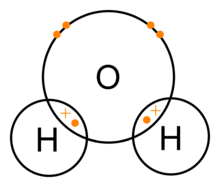
Covalente bindingen zijn chemische bindingen tussen twee niet-metalen atomen. Een voorbeeld is water, waar waterstof (H) en zuurstof (O) zich binden om te maken (H2O). Een volledige buitenste schil heeft meestal acht elektronen, of twee in het geval van waterstof of helium. Valentie-elektronen zijn de elektronen die relatief losjes in de buitenste schil van het atoom worden vastgehouden. De structuur van de elektronenhuiden wordt bepaald door de kwantummechanica).
Het aantal elektronen in een atoom wordt bepaald door het aantal protonen in het atoom. Elektronen draaien in een baan om de atoomkernen, en ze zijn als een soort van wazige orbitale paden rond een atoomkern. De eerste laag heeft tot twee elektronen. De lagen daarna bevatten meestal tot acht. Covalente bindingen worden gevormd door atomen die valentie-elektronen delen.
Als bijvoorbeeld een atoom negen elektronen had, dan draaien de eerste twee zeer dicht bij de kern, de volgende zeven iets verder weg. De buitenste zeven elektronen worden minder strak vastgehouden dan de binnenste twee elektronen omdat ze verder weg zijn van de positief geladen kern. Als dit atoom dicht bij een ander atoom komt, met een losjes gehouden elektron in zijn buitenste schil, zal een nieuwe baan beschikbaar komen voor het losjes gehouden elektron. Deze nieuwe elektronenbaan is gebonden aan beide atoomkernen en heeft een lager energieniveau dan de oorspronkelijke elektronenbaan. Het elektron kan er spontaan naartoe springen en met de overtollige energie een foton uitzenden. Nu hebben we een elektron dat in een baan om beide atomen draait waardoor het elektron een kleine netto positieve lading heeft en het andere atoom een kleine netto negatieve lading. De twee atomen worden nu bij elkaar gehouden door de elektromagnetische aantrekkingskracht tussen positieve en negatieve ladingen. Dit wordt een covalente binding genoemd. Om deze binding te verbreken is dezelfde hoeveelheid energie nodig als bij de vorming ervan is vrijgekomen.
Een watermolecuul bestaat uit een zuurstofatoom en twee waterstofatomen die door een covalente binding bij elkaar worden gehouden. In dit geval deelt het zuurstofatoom één elektron met elk waterstofatoom. Dit betekent dat het zuurstofatoom een kleine netto positieve lading heeft en het waterstofatoom een kleine netto negatieve lading. Hierdoor worden de zuurstof- en waterstofatomen naar elkaar aangetrokken door de elektromagnetische kracht. Hierdoor is het watermolecuul een polair molecuul: de lading is niet gelijkmatig verdeeld.