Atoombanen zijn de plaatsen rond de kern van een atoom waar de elektronen zich waarschijnlijk op een bepaald moment bevinden. Het is een wiskundige functie die het golfachtige gedrag van één van de elektronen of een paar elektronen in een atoom beschrijft.
Het woord 'orbitaal' wordt gebruikt omdat men dacht dat de elektronen zich op dezelfde manier gedroegen als het zonnestelsel, waarbij de kern als de zon is en de elektronen als de planeten in een baan om elkaar heen draaien.
Het aantal atoombanen in een element wordt bepaald door de periode waarin het element zich bevindt. Elektronen bewegen tussen de banen, afhankelijk van hoe snel ze bewegen en hoeveel andere elektronen er zijn.
In de atoomtheorie en de kwantummechanica is een atoombaan een kwantumnummer. Elk van deze banen kan worden bezet door één of twee elektronen. De manier waarop orbitalen worden gerangschikt is gerelateerd aan de elektronenconfiguraties van atomen. Zij werden afgeleid van beschrijvingen die door vroege spectroscopisten van bepaalde alkalimetaalspectroscopische lijnen als scherp, hoofd, diffuus, en fundamenteel worden verstrekt.
Kernbegrippen en kwantumnummers
Een orbitaal wordt volledig beschreven door vier kwantumnummers die voortkomen uit de oplossingen van de Schrödingergelijking (voor een waterstofachtig atoom):
- Hoofdkwantumgetal n (n = 1, 2, 3, ...): bepaalt de energie en de gemiddelde afstand van het elektron tot de kern (de schil).
- Azimutale kwantumgetal l (l = 0, 1, ..., n−1): bepaalt de vorm van het orbitaal. Elk l correspondeert met een lettersymbool: l = 0 → s, l = 1 → p, l = 2 → d, l = 3 → f, enz.
- Magnetisch kwantumgetal m_l (m_l = −l, ..., 0, ..., +l): geeft de oriëntatie van het orbitaal in de ruimte (aantal mogelijke oriëntaties = 2l+1).
- Spin kwantumgetal m_s (m_s = +1/2 of −1/2): geeft de spinrichting van het elektron aan. Per orbitaal kunnen maximaal twee elektronen met tegengestelde spin voorkomen (Pauli-uitsluitingsprincipe).
Vorm en aantal orbitalen
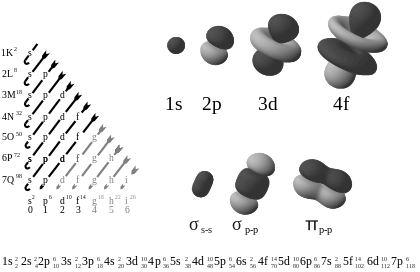
De meest bekende orbitaalvormen zijn:
- s-orbitalen (bolsymmetrisch, l = 0): elk energielevel heeft één s-orbitaal.
- p-orbitalen (haltervormig, l = 1): drie oriëntaties (m_l = −1, 0, +1), dus drie p-orbitalen per subschil.
- d-orbitalen (complexere vormen, l = 2): vijf oriëntaties per subschil.
- f-orbitalen (nog complexer, l = 3): zeven oriëntaties per subschil.
Elk orbitaal kan maximaal twee elektronen bevatten, dus een s-subshell bevat maximaal 2 elektronen, een p-subshell 6, een d-subshell 10 en een f-subshell 14.
Nodes, kansdichtheid en visualisatie
Een orbitaal is geen vaste baan maar een kansverdeling: de vierkantswortel van het kwadraat van de golffunctie geeft de elektrondichtheid of waarschijnlijkheid om een elektron op een bepaalde plaats aan te treffen. Orbitalen hebben
- radiale knopen (waar de waarschijnlijkheid op een bepaalde afstand van de kern nul is) en
- hoekknopen (gebieden waar de golffunctie van teken verandert).
Het aantal knopen neemt toe met n en l; visuele weergaven (isodichtheidsvlakken) tonen de karakteristieke vormen van s-, p-, d- en f-orbitalen.
Energiën en meer-elektron-atomen
Voor waterstofachtige atomen zijn de energieniveaus alleen afhankelijk van n. In meer-elektron-atomen beïnvloeden elektronen onderling elkaar via afscherming en uitwisseling, waardoor de volgorde van subshell-energieën verandert (bijvoorbeeld 4s kan een lagere energie hebben dan 3d). Daarom worden voor opbouw van grondtoestanden regels gebruikt zoals het Aufbau-principe, de Pauli-uitsluiting en de Hundse regel (elektronen bezetten eerst ongeladen gelijkwaardige orbitalen met gelijk spin).
Historische notatie en spectroscopie
De letters s, p, d en f komen van oude spectroscopische benamingen: sharp (scherp), principal (hoofd), diffuse (diffuus) en fundamental (fundamenteel). Die indeling weerspiegelt de manier waarop spektrallijnen werden geclassificeerd voordat de kwantummechanische verklaring bestond.
Keuze voor moleculen en chemische relevantie
In de chemie zijn orbitalen essentieel om bindingen te begrijpen: atomaire orbitalen combineren tot moleculaire orbitalen, en begrippen als hybridisatie (bijv. sp3, sp2) leggen uit hoe atomaire orbitalen zich mengen om bindingsrichtingen en -sterktes te bepalen. De vorm en energie van de buitenste orbitalen bepalen grotendeels de chemische eigenschappen van een element.
Samenvatting
- Een orbitaal is een wiskundige beschrijving van waar een elektron zich waarschijnlijk bevindt, niet een klassiek baantje.
- Orbitalen worden beschreven door vier kwantumnummers (n, l, m_l, m_s).
- Verschillende vormen (s, p, d, f) hebben verschillende oriëntaties en capaciteit voor elektronen.
- In meer-elektron-atomen zijn orbitalen benaderingen (gemiddelde velden) en bepaalt interactie tussen elektronen de energiereeks, wat chemische eigenschappen beïnvloedt.