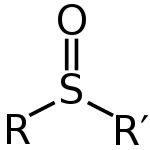
Een sulfoxide is een molecuul waarin een zwavelatoom gebonden is aan twee koolwaterstoffen en één zuurstofatoom. Het ontstaat bij de oxidatie van thioethers, zonder helemaal naar het sulfon te gaan. Zoals veel moleculen die zwavel bevatten, kan sulfoxide soms erg stinken.
Sulfoxiden kunnen worden geschreven met de algemene formule R-S(=O)-R'. Zwavel heeft een dubbele binding met de zuurstof, en een enkele binding met de koolwaterstoffen. Er blijft dus een lone pair over op het atoom. Dit betekent dat de vorm op dat atoom tetrahedraal is. Het betekent ook dat de zwavel een chiraal centrum kan zijn. Sulfoxiden worden gebruikt als goede liganden voor overgangsmetalen.
Een belangrijke molecule van dit type is dimethylsulfoxide. Het wordt ook wel DMSO genoemd. Het wordt gebruikt als oplosmiddel voor veel reacties, vooral in de biochemie.