Een hele vorm van chemie, organische chemie genaamd, gaat over koolstof en zijn verbindingen. Koolstof maakt vele soorten verbindingen. Koolwaterstoffen zijn moleculen met koolstof en waterstof. Methaan, propaan en vele andere brandstoffen zijn koolwaterstoffen. Veel van de stoffen die mensen dagelijks gebruiken zijn organische verbindingen.
Koolstof, waterstof, stikstof, zuurstof en enkele andere elementen zoals zwavel en fosfor vormen samen het meeste leven op aarde (zie Lijst van biologisch belangrijke elementen). Koolstof vormt een zeer groot aantal organische verbindingen omdat het sterke bindingen kan vormen met zichzelf en met andere elementen. Vanwege de hoeveelheid koolstof die levende dingen hebben, worden alle organische dingen beschouwd als "op koolstof gebaseerd".
Elk koolstofatoom vormt gewoonlijk vier chemische bindingen, die sterke verbindingen vormen met andere atomen om moleculen te vormen. Het soort binding dat koolstof maakt, wordt een covalente binding genoemd. Door deze bindingen kan koolstof vele soorten kleine en grote moleculen vormen. Een molecuul methaan is het kleinst; het heeft vier waterstofatomen gebonden aan koolstof. De bindingen kunnen dubbele bindingen zijn, wat betekent dat twee bindingen worden gevormd tussen koolstof en een ander atoom om een sterkere verbinding te maken. Koolstofdioxide heeft bijvoorbeeld twee zuurstofatomen, die elk een dubbele binding hebben met koolstof. Koolstof kan zelfs drie bindingen vormen met een ander atoom, een zogenaamde drievoudige binding. In het gas acetyleen bijvoorbeeld vormt koolstof een drievoudige binding met een ander koolstofatoom.
Door binding met andere koolstofatomen kan koolstof lange ketenvormige moleculen vormen, polymeren genaamd, zoals kunststoffen en eiwitten. Atomen van andere elementen kunnen deel uitmaken van de lange polymeerketens, vaak stikstof of zuurstof.
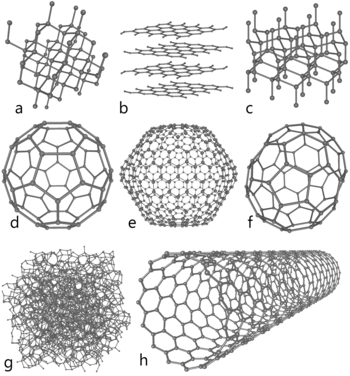
Zuivere koolstof vormt diamant door binding met vier andere koolstofatomen in een driedimensionaal kristal. Het vormt grafiet door binding met drie andere koolstofatomen tot dunne platte lagen.