Elektronenschil: uitleg, energieniveaus en elektronenconfiguratie
Elektronenschil uitleg: energieniveaus, subniveaus en elektronenconfiguratie helder uitgelegd met voorbeelden en formules — perfect voor studie en examenvoorbereiding.
Een elektronenschelp is het buitenste deel van een atoom rond de atoomkern. Het is de regio waar de elektronen zich bevinden en wordt in de kwantummechanica beschreven als een groep van atoombanen of orbitalen met dezelfde waarde van het hoofdkwantumnummer n. In oudere modellen, zoals het Bohr-model, werden deze schillen voorgesteld als vaste banen op bepaalde afstanden van de kern; de term "schelp" is uit dat model overgegaan in de moderne terminologie.
Structuur: subschalen en orbitalen
Elke elektronenschelp (gegeven door n) bevat een of meer elektronensubschalen (of kortweg subschalen). Een subschaal wordt gekenmerkt door het impulsmomentkwantumnummer l en heeft een vast aantal orbitalen. Voor een gegeven n geldt dat l waarden kan aannemen van 0 tot n−1. De gebruikelijke benamingen voor l-waarden zijn:
- l=0: s (1 orbitaal → maximaal 2 elektronen)
- l=1: p (3 orbitalen → maximaal 6 elektronen)
- l=2: d (5 orbitalen → maximaal 10 elektronen)
- l=3: f (7 orbitalen → maximaal 14 elektronen)
Het totaal aantal orbitalen in een schelp is n2, en het maximale aantal elektronen in die schelp is daarom 2 n2. Hetzelfde wordt vaak weergegeven met de formule:
Het aantal elektronen dat in een schelp kan zitten is gelijk aan 2 n 2. 
Kwantumgetallen en betekenis
- Hoofdkwantumgetal (n): bepaalt de schelpniveau en grotendeels de energie bij waterstofachtige systemen; n = 1, 2, 3, ...
- Impulsmomentkwantumgetal (l): bepaalt de vorm van de orbitaal (s, p, d, f, ...)
- Magnetisch kwantumgetal (m): specificeert de oriëntatie van een orbitaal binnen een subschaal
- Spinkwantumgetal (ms): geeft de spinrichting van een elektron aan (+1/2 of −1/2)
Energieniveaus en invulling (regelgeving)
In meerelektronensystemen heeft niet elke schelp voor alle elementen dezelfde energie: binnen en tussen schillen kunnen subschalen in energie overlappen. Een praktische regel om de volgorde van invulling te bepalen is de Madelung- of n + l-regel: subschalen met lagere waarde van (n + l) worden doorgaans eerst gevuld; bij gelijke (n + l) heeft de subschaal met lagere n de voorkeur. Voorbeelden van de volgorde zijn:
- 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p ...
Belangrijke principes die de elektroneninvulling bepalen:
- Opvulregel (Aufbau-principe): elektronen vullen de laagste beschikbare energieniveaus eerst.
- Pauli-uitsluitingsprincipe: in één orbitaal kunnen maximaal twee elektronen voorkomen met tegengestelde spin.
- Hund-regel: binnen een subschaal bezetten elektronen eerst zoveel mogelijk verschillende orbitalen met parallelle spin voordat paren worden gevormd.
Sommige elementen tonen afwijkingen van de verwachte volgorde (vooral bij overgangsmetalen en zwaardere elementen), bijvoorbeeld Cr en Cu vanwege extra stabiliteit van halfgevulde of volledig gevulde d-subshells.
Valentieschil en chemische eigenschappen
De buitenste elektronenschelp (valentieschil) bepaalt in sterke mate de chemische eigenschappen van een element: het aantal valentie-elektronen beïnvloedt bindingstype, reactiviteit en de plaats in het periodiek systeem. Bijvoorbeeld:
- De edelgassen hebben volledig gevulde buitenste schillen en zijn chemisch inert.
- De alkalimetalen hebben één valentie-elektron en reageren gemakkelijk door dat elektron af te geven.
Voorbeelden
- n = 1 (K-schil): alleen 1s, maximaal 2 elektronen.
- n = 2 (L-schil): 2s en 2p, maximaal 8 elektronen (2·2² = 8).
- n = 3 (M-schil): 3s, 3p, 3d, maximaal 18 elektronen.
Samenvattend
Een elektronenschelp is een kwantummechanisch energieniveau rond de kern, opgebouwd uit subschalen en orbitalen. De maximale capaciteit van een schelp is 2 n2 elektronen. Hoewel de term uit het Bohr-model stamt, wordt in de moderne chemie en natuurkunde meer gewerkt met orbitalen en kwantumgetallen om positie en energie van elektronen nauwkeurig te beschrijven.
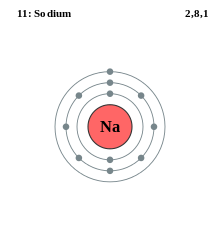
Voorbeeld van een model van een natriumelektronenschaal met drie schalen
Valentieschaal
De valentieschaal is de buitenste schil van een atoom in zijn ongecombineerde staat, die de elektronen bevat die het meest waarschijnlijk verantwoordelijk zijn voor de aard van eventuele reacties met betrekking tot het atoom en van de bindingsinteracties die het heeft met andere atomen. Er moet op worden gelet dat het buitenste omhulsel van een ion niet algemeen als valentieomhulsel wordt aangeduid. Elektronen in de valentiemantel worden valentie-elektronen genoemd.
In een edelgas heeft een atoom de neiging om 8 elektronen in zijn buitenste schil te hebben (behalve helium, dat slechts in staat is om zijn schil met 2 elektronen te vullen). Dit dient als model voor de octet-regel die vooral van toepassing is op de hoofdgroepelementen van de tweede en derde periode. In termen van atoombanen zijn de elektronen in de valentiemantel verdeeld over 2 in de enkele s-baan en 2 in de drie p-baan.
Voor coördinatiecomplexen die overgangsmetalen bevatten, bestaat de valentiemantel uit elektronen in deze s- en p-circuits, evenals maximaal 10 extra elektronen, verdeeld als 2 in elk van 5 d-circuits, om een totaal van 18 elektronen in een volledige valentiemantel voor zo'n samenstelling te maken. Dit wordt de regel van achttien elektronen genoemd.
| Mogelijk aantal elektronen in de schelpen 1-5 | |
| Shell | Elektronen |
| 1 | 2 |
| 2 | 8 |
| 3 | 18 |
| 4 | 32 |
| 5 | 32 |
| 6 | 18 |
| 7 | 8 |
Subshells
Electronische subschalen worden geïdentificeerd met de letters s, p, d, f, g, h, i, enz., die overeenkomen met de azimuthal-kwantumnummers (l-waarden) 0, 1, 2, 3, 4, 5, 6, enz. Elk omhulsel kan respectievelijk 2, 6, 10, 14 en 18 elektronen bevatten, of 2(2l + 1) elektronen in elk omhulsel. De notatie 's', 'p', 'd', en 'f' zijn afkomstig van een inmiddels geaccrediteerd systeem van het categoriseren van spectraallijnen als "scherp", "hoofd", "diffuus", of "fundamenteel", op basis van hun waargenomen fijne structuur. Toen de eerste vier soorten orbitalen werden beschreven, werden ze geassocieerd met deze spectraallijntypen, maar er waren geen andere namen. De benamingen 'g', 'h', enzovoorts, werden afgeleid door de alfabetische volgorde te volgen.
Vragen en antwoorden
V: Wat is een elektronenschil?
A: Een elektronenschil, of hoofd-energieniveau, is het deel van een atoom waar elektronen zich in een baan om de atoomkern bevinden.
V: Hoeveel elektronen kunnen zich in een bepaalde schil bevinden?
A: Het aantal elektronen dat zich in een bepaalde schil kan bevinden, is gelijk aan 2n2.
V: Wat zegt het Bohr-model over elektronen?
A: Het Bohr-model stelt dat elektronen op bepaalde afstanden om de kern draaien, zodat hun banen "schillen" vormen.
V: Wie heeft deze term voorgesteld?
A: Deze term werd gepresenteerd door Niels Henrik David Bohr.
V: Waaruit bestaat de elektronenconfiguratie van een atoom?
A: Elektronenschillen vormen de elektronenconfiguratie van een atoom.
V: Bestaan alle atomen uit één of meer elektronenschillen?
A: Ja, alle atomen hebben één of meer elektronenschillen.
V: Hebben alle elektronenschillen verschillende aantallen elektronen?
A: Ja, alle elektronenschillen hebben een verschillend aantal elektronen.
Zoek in de encyclopedie