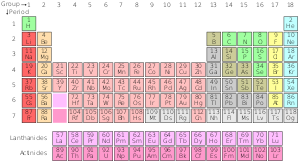
Het periodiek systeem van de chemische elementen is een lijst van bekende chemische elementen. In de tabel zijn de elementen geplaatst in de volgorde van hun atoomnummer, beginnend met het laagste nummer van één, waterstof. Het atoomnummer van een element is hetzelfde als het aantal protonen in die specifieke atoomkern. In het periodiek systeem zijn de elementen gerangschikt in perioden en groepen. Een rij elementen over de tabel heen wordt een periode genoemd. Elke periode heeft een getal; van 1 tot 8. Periode 1 heeft slechts 2 elementen: waterstof en helium. Periode 2 en periode 3 hebben allebei 8 elementen. Andere perioden zijn langer. Elementen in een periode hebben opeenvolgende atoomnummers.
Een kolom met elementen in de tabel wordt een groep genoemd. Er zijn 18 groepen in het standaard periodiek systeem. Elke groep heeft een nummer: van 1 tot 18. Elementen in een groep hebben elektronen die op vergelijkbare wijze gerangschikt zijn, afhankelijk van het aantal valentie-elektronen, waardoor ze vergelijkbare chemische eigenschappen hebben (ze gedragen zich op vergelijkbare wijze). Groep 18 staat bijvoorbeeld bekend als de edelgassen, omdat het allemaal gassen zijn en ze niet combineren met andere atomen.
Er zijn twee systemen van groepsnummers; een met Arabische cijfers (1,2,3) en de andere met Romeinse cijfers (I, II, III). De Romeinse cijfers werden in het grootste deel van de 20e eeuw gebruikt. In 1990 besloot de International Union of Pure and Applied Chemistry (IUPAC) het nieuwe systeem te gebruiken met Arabische cijfers, ter vervanging van de twee oude groepssystemen die Romeinse cijfers gebruikten.
Het periodiek systeem is door chemici gebruikt om patronen en relaties tussen elementen te observeren. Er zijn 3 hoofdgroepen in het periodiek systeem; metalen, metalloïden en niet-metalen. Zo zijn bijvoorbeeld elementen onder en ver links van de tabel het meest metaalachtig, en elementen rechtsboven het minst metaalachtig. (b.v. cesium is veel meer metaalachtig dan helium). Er zijn ook veel andere patronen en relaties.
Het periodiek systeem is uitgevonden door de Russische chemicus Dmitri IvanovitsjMendeleyev (1834-1907). Ter zijner ere werd element 101 naar hem vernoemd, mendeljevium.