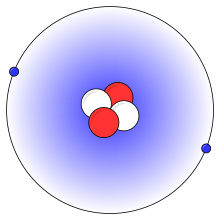
Grootte en massa
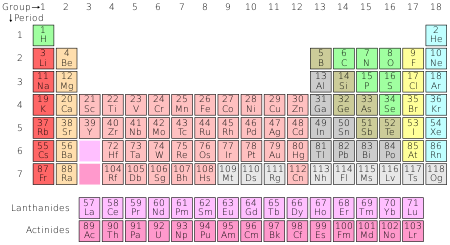
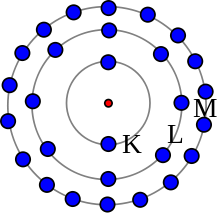
De grootte van een atoom hangt af van de grootte van zijn elektronenwolk. Naar beneden in het periodiek systeem worden meer elektronenschillen toegevoegd. Daardoor worden atomen groter. Naar rechts in het periodiek systeem worden meer protonen aan de kern toegevoegd. Er worden echter geen elektronenschillen toegevoegd. Deze positievere kern trekt sterker aan elektronen, waardoor atomen kleiner worden. Het grootste atoom is cesium, dat volgens één model ongeveer 0,596 nanometer breed is. Het kleinste atoom is helium, dat ongeveer 0,062 nanometer breed is.
De massa van atomen varieert van 1,7×10−24 tot 4,9×10 −22gram. Meestal wordt de massa gemeten met de atoommassa-eenheid (amu), ook wel dalton genoemd. Eén amu is precies 1/12 van de massa van een koolstof-12 atoom, die 1,7×10−24 gram bedraagt. Waterstof-1 heeft een massa van ongeveer 1 amu, en het zwaarste bekende atoom, oganesson, heeft een massa van ongeveer 294 amu.
Hoe atomen op elkaar inwerken
Als atomen ver uit elkaar liggen, trekken ze elkaar aan. Deze aantrekkingskracht is voor sommige soorten atomen sterker dan voor andere. Tegelijkertijd zorgt de warmte, of kinetische energie, van atomen ervoor dat ze voortdurend bewegen. Als de aantrekkingskracht sterk genoeg is in verhouding tot de hoeveelheid warmte, vormen de atomen een vaste stof. Als de aantrekkingskracht zwakker is, vormen ze een vloeistof, en als de aantrekkingskracht nog zwakker is, vormen ze een gas.
Chemische bindingen zijn de sterkste vormen van aantrekkingskracht tussen atomen. Bij alle chemische bindingen worden elektronen verplaatst. Atomen verbinden zich gewoonlijk met elkaar op een manier die hun buitenste elektronenschil vult of leegt. De meest reactieve elementen moeten een klein aantal elektronen verliezen of winnen om een volle buitenste schil te hebben. Atomen met een volle buitenste schil, edelgassen genoemd, vormen gewoonlijk geen bindingen.
Er zijn drie belangrijke soorten bindingen: ionische bindingen, covalente bindingen en metaalbindingen.
- Bij een ionische binding geeft een atoom elektronen aan een ander atoom. Elk atoom wordt een ion: een atoom of groep atomen met een positieve of negatieve lading. Het positieve ion (dat elektronen heeft verloren) wordt een kation genoemd; het is meestal een metaal. Het negatieve ion (dat elektronen heeft gewonnen) wordt een anion genoemd; het is meestal een niet-metaal. Ionische binding resulteert meestal in een rooster, of kristal, van bij elkaar gehouden ionen.
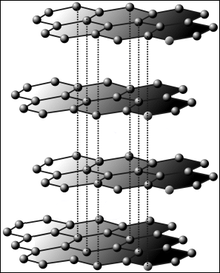
- Bij een covalente binding delen twee atomen elektronen. Dit gebeurt meestal wanneer beide atomen niet-metalen zijn. Covalente bindingen vormen vaak moleculen, variërend in grootte van twee atomen tot veel meer. Ze kunnen ook grote netwerken vormen, zoals glas of grafiet. Het aantal bindingen dat een atoom maakt (zijn valentie) is meestal het aantal elektronen dat nodig is om zijn buitenste elektronenschil te vullen.
- In een metaalbinding bewegen elektronen vrij tussen vele metaalatomen. Elk aantal atomen kan zich op deze manier binden. Metalen geleiden elektrische stroom omdat er gemakkelijk elektrische lading doorheen kan stromen. Atomen in metalen kunnen langs elkaar heen bewegen, zodat metalen gemakkelijk kunnen worden gebogen, uitgerekt en vervormd.
Alle atomen trekken elkaar aan door Van der Waals-krachten, die zwakker zijn dan chemische bindingen. Deze krachten worden veroorzaakt wanneer elektronen naar één kant van een atoom bewegen. Deze beweging geeft een negatieve lading aan die kant. Het geeft ook een positieve lading aan de andere kant. Wanneer twee atomen hun zijden met negatieve en positieve lading op één lijn brengen, trekken ze elkaar aan.
Ondanks het feit dat atomen voornamelijk uit lege ruimte bestaan, kunnen zij elkaar niet passeren. Wanneer twee atomen zich zeer dicht bij elkaar bevinden, zullen hun elektronenwolken elkaar afstoten door de elektromagnetische kracht.
Magnetisme
Een elektron heeft een eigenschap die magnetisch moment wordt genoemd en die een richting en een grootte (of omvang) heeft. Het magnetisch moment komt voort uit de individuele spin van het elektron en zijn baan rond de kern. Samen vormen de magnetische momenten van de elektronen een magnetisch moment voor het hele atoom. Dit verklaart het gedrag van atomen in een magnetisch veld.
Elk elektron in een atoom heeft een van de twee soorten spin. Als elk elektron wordt gekoppeld aan een elektron met de tegenovergestelde spin, heffen de spins op, zodat het atoom geen blijvend magnetisch moment heeft. Dergelijke atomen worden diamagnetisch genoemd: ze worden slechts zwak afgestoten door een magnetisch veld.
Als sommige elektronen echter niet gekoppeld zijn, heeft het atoom een blijvend magnetisch moment: het is dan paramagnetisch of ferromagnetisch. Wanneer atomen paramagnetisch zijn, wijst het magnetisch moment van elk atoom in een willekeurige richting. Ze worden zwak aangetrokken door een magnetisch veld. Wanneer atomen ferromagnetisch zijn, werken de magnetische momenten van nabijgelegen atomen op elkaar in. Ze wijzen in dezelfde richting. In een magnetisch veld zullen de meeste atomen in de richting van het veld wijzen. Ferromagnetische materialen, zoals ijzer, kobalt en nikkel, worden sterk aangetrokken door een magnetisch veld.
Radioactief verval
Sommige elementen, en veel isotopen, hebben een zogenaamde onstabiele kern. Dit betekent dat de kern ofwel te groot is om zichzelf bij elkaar te houden, ofwel te veel protonen of neutronen heeft. Wanneer dit gebeurt, moet de kern de overtollige massa aan deeltjes verwijderen. Dit doet hij door middel van straling. Een atoom dat dit doet, wordt radioactief genoemd. Instabiele atomen zenden straling uit totdat ze genoeg deeltjes in de kern verliezen om stabiel te worden. Alle atomen boven atoomnummer 82 (82 protonen, lood) zijn radioactief.
Er zijn drie belangrijke soorten radioactief verval: alfa, bèta en gamma.
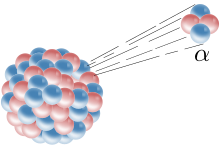
- Bij alfaverval schiet het atoom een deeltje met twee protonen en twee neutronen naar buiten. Dit is in wezen een heliumkern. Het resultaat is een element met een atoomnummer twee minder dan voorheen. Als bijvoorbeeld een berylliumatoom (atoomnummer 4) een alfaverval doormaakt, wordt het helium (atoomnummer 2). Alfaverval treedt op wanneer een atoom te groot is en zich van wat massa moet ontdoen.
- Bij bètaverval verandert een neutron in een proton, of een proton in een neutron. In het eerste geval schiet het atoom een elektron uit. In het tweede geval is het een positron (zoals een elektron, maar met een positieve lading). Het resultaat is een element met één hoger of één lager atoomnummer dan voorheen. Bètaverval treedt op wanneer een atoom te veel protonen of te veel neutronen heeft.
- Er is sprake van gammaverval wanneer een atoom een gammastraal, of golf, uitstraalt. Dit gebeurt wanneer de energie van de kern verandert. Dit gebeurt meestal nadat een kern het alfa- of bètaverval heeft doorlopen. Er is geen verandering in de massa of het atoomnummer van het atoom, alleen in de opgeslagen energie in de kern, in de vorm van de spin van de deeltjes.
Elk radioactief element of isotoop heeft een halveringstijd. Dit is hoe lang het duurt voordat de helft van een monster atomen van dat type vervalt tot ze een ander isotoop of element worden.
Splijting en fusie
Apparaten die gebruik maken van kernsplijting beginnen met het afschieten van neutronen op atomen. Hierdoor valt het atoom snel uit elkaar. De splitsing van één atoom schiet meer neutronen af, die vervolgens andere atomen breken, waardoor kettingreacties ontstaan. Dit proces levert enorme hoeveelheden warmte-energie op. De kettingreactie van kernsplijting dreef de eerste kernwapens (splijtingsbommen) aan. Kerncentrales zijn een beetje anders: er worden zogenaamde regelstaven gebruikt om de splijting te vertragen. Regelstaven vangen een deel van de neutronen op, waardoor een kettingreactie wordt voorkomen.
Kernfusie komt vooral voor in de zon en andere sterren. Het vereist een hete plaats, maar levert nog meer energie op dan kernsplijting. Dit verklaart de hitte en het licht van de zon. De zon fuseert nu waterstof tot helium, terwijl grotere en hetere sterren zwaardere atomen maken. Fusiebommen, of thermonucleaire wapens, zijn de krachtigste kernwapens. Wetenschappers proberen fusiereactoren te maken voor kerncentrales, maar er bestaat nog geen enkele.
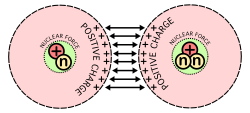
Kernfusie en kernsplijting produceren om vergelijkbare redenen energie. Volgens Einsteins beroemde formule E = mc2 kan een kleine hoeveelheid massa worden omgezet in een grote hoeveelheid energie. Wanneer protonen en neutronen bij kernfusie samenkomen, verliezen ze wat massa, die ze als energie uitzenden. De kern kan zich alleen splitsen in zijn protonen en neutronen als dezelfde hoeveelheid energie wordt toegevoegd. Deze eigenschap van elk type kern wordt zijn nucleaire bindingsenergie genoemd. Fusie of splitsing zenden energie uit als de totale bindingsenergie toeneemt. Kernen in het bereik van ijzer-56 en nikkel-62 hebben de hoogste bindingsenergie gedeeld door hun aantal protonen en neutronen, zodat zij over het algemeen geen splitsing of fusie ondergaan. Grotere atomen, zoals uranium, ondergaan kernsplijting, omdat hun bindingsenergie daardoor toeneemt.