Het plumpuddingmodel was een vroeg (en onjuist) 20e eeuws model van een atoom. Het werd voorgesteld door J.J. Thomson in 1904, na de ontdekking van het elektron, maar vóór de ontdekking van de atoomkern. In die tijd wisten wetenschappers dat er een positieve lading in het atoom was die de negatieve lading van de elektronen compenseerde, waardoor het atoom neutraal was, maar zij wisten niet waar de positieve lading vandaan kwam. Het model van Thomson toonde een atoom met een positief geladen medium, of ruimte, met negatief geladen elektronen binnen het medium. Al snel na zijn voorstel werd het model het 'plum pudding'-model genoemd, omdat het positieve medium op een pudding leek, met elektronen, of pruimen, erin.
Atoommodel van Thomson
Ontwikkeling tot modern atoommodel
Rutherford's model
In 1909, niet lang nadat het model van Thomson was voorgesteld, deden Hans Geiger en Ernest Marsden een experiment met dunne plaatjes goud, om het model van Thomson te testen. Hun professor, Ernest Rutherford, verwachtte dat de resultaten zouden bewijzen dat Thomson gelijk had, maar de resultaten waren heel anders dan zij verwachtten. In 1911 ontdekte Rutherford dat de positieve ladingen afkomstig waren van kleine deeltjes, protonen genaamd, en dat de protonen zich in een klein centrum bevonden, de kern genaamd, en dat de elektronen om de kern heen draaiden.
Bohr-model
Rutherfords model was vrij eenvoudig, maar het was verkeerd omdat elektronen lading hebben, en zij zouden moeten worden aangetrokken door de positief geladen kern. In 1913 voegde Niels Bohr 'energieniveaus' toe aan het atoommodel. Elektronen vallen niet in de kern omdat ze in energieniveaus zitten, en om naar hogere energieniveaus te gaan is extra energie nodig, en om naar lagere energieniveaus te gaan is een afgifte van energie nodig. Het is niet mogelijk van energietoestand te veranderen zonder de energie van het elektron te veranderen. Als een elektron wordt geraakt door een foton (een deeltje dat elektromagnetische straling uitzendt) zal het extra energie krijgen en naar een hoger energieniveau gaan (het verandert van toestand), daarna zal het terugspringen naar een lager energieniveau, waarbij de ingesloten energie vrijkomt. Dit nieuwe model werd het Bohr-model of het Rutherford-Bohr-model genoemd. Dit voegde een geheel nieuwe tak van wetenschap toe: Kwantumfysica.
Kwantum model
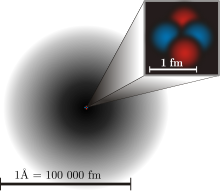
In 1926 gebruikte Erwin Schrödinger het idee dat elektronen zowel als golf als als deeltje fungeerden, dit staat bekend als golf-deeltje dualiteit. Dit voegde een geheel nieuwe laag toe aan het atoommodel en de kwantumfysica. Bij een deeltje kun je weten waar het zich in de ruimte bevindt als je het waarneemt (er naar kijkt). Maar bij een golf is het overal, zodat je niet kunt bepalen waar het zich precies bevindt. Dit staat bekend als kwantumonzekerheid. Bij een elektron kun je alleen de waarschijnlijkheid weten dat het zich op een bepaalde plaats bevindt, omdat het zowel een golf als een deeltje is. (Zie diagram hierboven)