In de scheikunde en de natuurkunde verklaart de atoomtheorie hoe ons begrip van het atoom in de loop der tijden is veranderd. Atomen werden vroeger beschouwd als de kleinste deeltjes van materie. Nu weet men echter dat atomen zijn opgebouwd uit protonen, neutronen en elektronen. Deze subatomaire deeltjes zijn opgebouwd uit quarks. Het eerste idee van het atoom kwam van de Griekse filosoof Democritus. Veel van de ideeën in de moderne theorie zijn afkomstig van John Dalton, een Brits scheikundige en natuurkundige.
De theorie is van toepassing op vaste stoffen, vloeistoffen en gassen, maar niet op een wijze die analoog is aan plasma's of neutronensterren.
Wat is de atoomtheorie?
De atoomtheorie is het wetenschappelijke kader dat verklaart wat atomen zijn, hoe ze zijn opgebouwd en hoe ze zich gedragen. Ze beschrijft onder meer:
- de samenstelling van atomen (kern en elektronenwolk),
- de eigenschappen van subatomaire deeltjes (massa, lading, spin),
- hoe atomen reageren en binden om moleculen te vormen,
- en hoe kwantummechanica het gedrag van elektronen bepaalt.
Korte geschiedenis en belangrijke modellen
De opvatting over het atoom ontwikkelde zich stap voor stap:
- Democritus (ca. 5e eeuw v.Chr.): stelde het idee voor van ondeelbare deeltjes, de 'atomos'.
- John Dalton (begin 19e eeuw): herintroduceerde het idee van discrete atomen en stelde een eenvoudige atoomtheorie op die massabehoud en vaste verhoudingen in chemische reacties verklaarde.
- J.J. Thomson (1897): ontdekte het elektron en stelde het 'plumpudding'-model voor, waarin elektronen in een positieve massa waren ingebed.
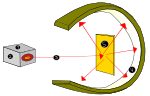
- Ernest Rutherford (1911): uit goudfolie-experimenten bleek dat bijna alle massa geconcentreerd is in een klein, positief geladen kern, waarmee het kernmodel ontstond.
- Niels Bohr (1913): introduceerde gekwantiseerde elektronbanen voor waterstof om spectra te verklaren; dat model werkt goed voor eenvoudige atomen.
- Kwantummechanisch model (20e eeuw): met bijdragen van Schrödinger, Heisenberg en anderen werd het klassieke beeld vervangen door een probabilistisch beeld van orbitalen en golffuncties — elektronen zijn verspreide ladingwolken met waarschijnlijkheidsverdelingen.
- Ontdekking van de neutron (James Chadwick, 1932): verklaarde isotopen en completes het beeld van de kern.
Samenstelling van atomen
Een typisch atoom bestaat uit twee hoofdonderdelen:
- Kern: zeer klein (~10⁻¹⁵ meter), maar bevat bijna de gehele massa van het atoom. In de kern bevinden zich protonen (positieve lading) en neutronen (geen elektrische lading). Protonen en neutronen worden samen nucleonen genoemd en zijn opgebouwd uit quarks (vooral up- en down-quarks) die door de sterke kernkracht bijeengehouden worden.
- Elektronenwolk: elektronen (negatief geladen) bewegen rond de kern in orbitalen. De grootte van de elektronenwolk is typisch ~10⁻¹⁰ meter, veel groter dan de kern. Elektronen bepalen grotendeels de chemische eigenschappen van een atoom en hoe atomen binden tot moleculen.
Belangrijke begrippen:
- Atoomnummer (Z): aantal protonen in de kern; bepaalt het element (bijv. Z=1 is waterstof).
- Massagetal (A): som van protonen en neutronen; isotopen van een element verschillen in A.
- Ionen: atomen die elektronen hebben verloren of gewonnen en daardoor elektrisch geladen zijn.
Fundamentele krachten en interacties
Verschillende natuurkrachten zijn belangrijk op atomaire schaal:
- Elektromagnetische kracht: houdt elektronen gebonden aan de kern en bepaalt chemische bindingen.
- Sterke kernkracht: bindt quarks in protonen/neutronen en bindt nucleonen in de kern, ondanks de elektrische afstoting tussen protonen.
- Zwakke kernkracht: speelt een rol bij bepaalde vormen van radioactief verval.
Toepassingen en bewijs
De atoomtheorie is de basis voor veel technologieën en vakgebieden:
- Chemie: verklaring van reacties, bindingen en de periodieke tabel.
- Materiaalkunde: begrip van kristalstructuren en elektrische eigenschappen.
- Nucleaire technologie: kernenergie en beeldvormingstechnieken (PET, röntgencontrasten).
- Meetmethoden: verspreidingsexperimenten (zoals Rutherford), spectroscopie, elektronenmicroscopie en deeltjesversnellers geven direct of indirect bewijs voor de structuur van atomen en subatomaire deeltjes.
Beperkingen en uitzonderingen
De atoomtheorie geldt zeer goed voor vaste stoffen, vloeistoffen en gassen, maar in sommige extreme toestanden verandert de geldigheid of de toepasbaarheid van het woord 'atoom':
- Plasma's: sterk geïoniseerde gassen waarin elektronen grotendeels los zijn van kernen; chemische concepten werken hier anders omdat veel deeltjes vrij bewegen.
- Neutronensterren: extreem samengetrokken materie waar atomen worden verpletterd en materie grotendeels uit neutronen bestaat; de gebruikelijke atomaire structuren bestaan daar niet meer.
Samenvattend
De atoomtheorie is een evoluerend wetenschappelijk raamwerk dat van klassieke ideeën (Dalton) via kernmodellen (Rutherford, Bohr) naar het moderne kwantummechanische beeld is gegroeid. Atomen zijn geen ondeelbare bolletjes meer, maar complexe systemen met een compacte kern en een wijdverspreide elektronenwolk, opgebouwd uit protonen, neutronen en elektronen — en op een dieper niveau uit quarks en fundamentele krachten.