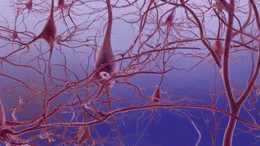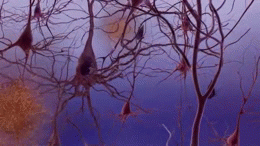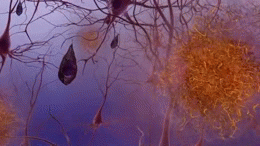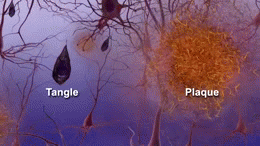
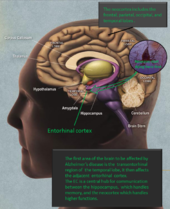
Twee van de belangrijkste kenmerken van de hersenen van mensen met de ziekte van Alzheimer zijn neurobrillaire tangles ("tangles"), die bestaan uit een eiwit dat tau wordt genoemd, en seniele plaques (die meestal bestaan uit een ander eiwit dat beta-amyloïde wordt genoemd, en soms ook beta-amyloïde bundels of kortweg "bundels" worden genoemd). De tau-eiwitten die de klitten vormen, hielden voorheen een structuur in de neuronen bijeen die microtubule heet en een belangrijk onderdeel is van het neuron; het maakt deel uit van het cytoskelet (celskelet) dat de vorm van een cel in stand houdt, en microtubules spelen een rol in de celcommunicatie.
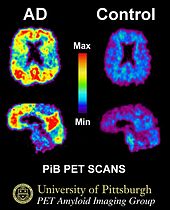
Zowel klitten als plaques kunnen worden veroorzaakt door andere ziekten, zoals het Herpes simplex virus type 1, dat wordt onderzocht als mogelijke oorzaak van of bijdrage aan het ontstaan van Alzheimer. Het is niet zeker of klitten en plaques deel uitmaken van wat Alzheimer veroorzaakt, of dat ze het gevolg zijn.
Microtubuli 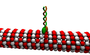
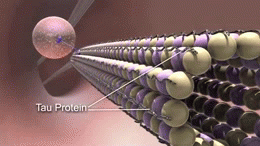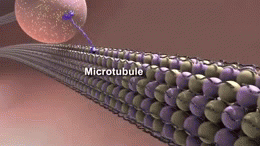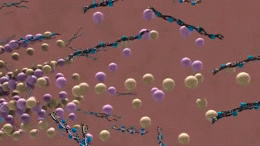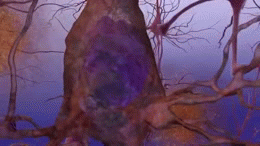
Microtubuli zijn gemaakt van een eiwit dat tubuline heet. De tubuline wordt gepolymeriseerd, wat betekent dat moleculen steeds weer dezelfde vormen aannemen die in groepen aan elkaar worden gekoppeld. Ze kunnen lange ketens of andere vormen vormen; in dit geval vormt de gepolymeriseerde tubuline microtubuli. De microtubuli zijn stijve buizen zoals microscopische rietjes die hol zijn van binnen. Microtubuli helpen de vorm van het neuron te behouden en zijn betrokken bij het doorgeven van signalen door het neuron.
Tau 
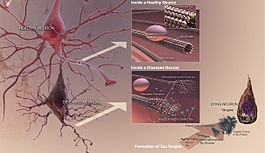
Tau is een eiwit dat vooral voorkomt in de neuronen van het centrale zenuwstelsel. Ze helpen de microtubuli in de neuronen bijeen te houden. Als er veranderingen optreden in de manier waarop de tau-eiwitten moeten werken, vallen de microtubuli uit elkaar. De tau-eiwitten die de microtubuli niet langer bij elkaar houden, vormen strengen, fibrillen genaamd, die vervolgens in het neuron samenklonteren tot zogenaamde neurofibrillaire klonters. Deze klonters, ook bekend als "tau-tangles", zijn alles wat overblijft nadat een neuron is afgestorven.
| Braak Staging van aan de ziekte van Alzheimer gerelateerde neurofibrillaire veranderingen.
Dit wordt momenteel alleen gebruikt voor onderzoeksdoeleinden |
| Stadium | Neurofibrillaire klitten in: | Symptomen |
| I/II
Transentorhinaal stadium | Transentorhinale regio en entorhinale regio | Geen symptomen |
| III/IV
Limbisch stadium
| Hippocampusformatie en delen van het limbisch systeem en de amygdala | Beginnende ziekte van Alzheimer
Cognitieve stoornissen: geheugenproblemen, ruimtelijke cognitie |
| V/VI
Isocorticaal stadium | In de hele hersenschors | Dementie: volledig ontwikkelde ziekte van Alzheimer |
Beta-amyloïde 
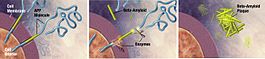
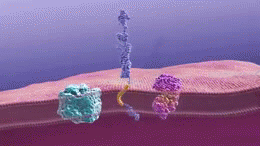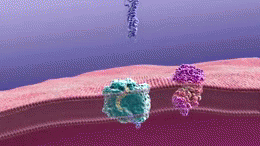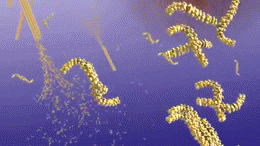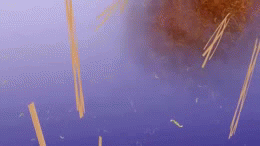
Beta-amyloïde(Aβ) (ook wel 'amyloïde-bèta' genoemd) plaques beginnen met een eiwit dat amyloïde precursor-eiwit (APP) heet. APP is een van de eiwitten waaruit het membraan of de buitenste laag van een cel bestaat, die de cel beschermt. In dit geval een neuron. Omdat het in de cel wordt gemaakt, steekt APP door het membraan van de cel heen.
In verschillende delen van de cel, waaronder het buitenste deel van het celmembraan, knippen chemische stoffen, enzymen genaamd, het APP in kleine stukjes. Deze enzymen zijn alfa-secretase, beta-secretase en gamma-secretase. Afhankelijk van welk enzym het knippen doet en welke delen van het APP worden geknipt, kunnen er twee verschillende dingen gebeuren. Het ene is nuttig en het andere veroorzaakt de vorming van beta-amyloïde plaques.
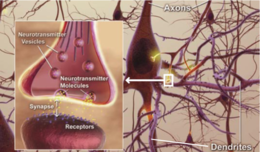
De plaques worden gevormd wanneer beta-secretase het APP-molecuul aan één uiteinde van het beta-amyloïde peptide doorsnijdt, waardoor sAPPβ uit de cel vrijkomt. Gamma-secretase knipt vervolgens de stukjes APP die overblijven en die nog uit het membraan van het neuron steken, aan het andere uiteinde van het beta-amyloïde peptide. Na dit knippen komt het beta-amyloïde peptide vrij in de ruimte buiten het neuron en begint aan andere beta-amyloïde peptiden te kleven. Deze stukjes plakken aan elkaar tot oligomeren. Verschillende oligomeren van verschillende grootte zweven nu rond in de ruimte tussen de neuronen, die mogelijk reageren met receptoren op naburige cellen en synapsen, waardoor hun vermogen om te functioneren wordt aangetast.
Sommige van deze oligomeren worden uit de hersenen verwijderd. De oligomeren die niet worden opgeruimd, klonteren samen met andere stukjes beta-amyloïde. Naarmate meer stukjes samenklonteren, worden de oligomeren groter, en de volgende grootte wordt protofibrillen genoemd en de volgende grootte daarna fibrillen. Na verloop van tijd klonteren deze fibrillen samen met andere eiwitmoleculen, neuronen en niet-zenuwcellen die in de ruimte tussen de cellen rondzweven, en vormen zo zogenaamde plaques.
Cerebrale amyloïde angiopathie (CAA)
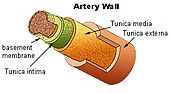
Afzettingen van beta-amyloïd worden ook gevormd in de wanden (in de tunica media, de middelste laag, en de tunica adventitia of tunica externa, de buitenste laag) van kleine en middelgrote slagaders (en soms aders) in de hersenschors en de leptomeninges (de leptomeninges zijn de twee binnenste lagen - pia mater en arachnoïd - van de hersenvliezen, een beschermend membraan met drie lagen dat de hersenen bedekt).
CAA wordt aangetroffen bij 30% van de mensen boven de 60 jaar die geen dementie hebben, maar komt voor bij 90%-96% van de mensen met de ziekte van Alzheimer en is in een derde tot twee derde van deze gevallen ernstig.


-MRI.png)