PH
De pH is een schaal met een zuurgraad van 0 tot 14. Het vertelt hoe zuur of basisch een stof is. Meer zure oplossingen hebben een lagere pH. Meer alkalische oplossingen hebben een hogere pH. Stoffen die niet zuur of alkalisch zijn (dus neutrale oplossingen) hebben meestal een pH van 7. Zuren hebben een pH die lager is dan 7. Alkaliën hebben een pH-waarde die hoger is dan 7.
pH is een maat voor de concentratie van protonen (H+) in een oplossing. S.P.L. Sørensen introduceerde dit concept in het jaar 1909. De p staat voor de Duitse potentie, dat wil zeggen vermogen of concentratie, en de H voor het waterstofion (H+).
De meest voorkomende formule voor het berekenen van de pH is:
pH = - log 10 [ H + ] {\mbox{pH}}=-log _10}links [{\mbox{H}}}^^+right]}
[H+] geeft de concentratie van H+-ionen aan (ook wel geschreven [H3O+], de gelijke concentratie van hydronium-ionen), gemeten in mollen per liter (ook wel molariteit genoemd).
Maar de juiste vergelijking is eigenlijk wel:
pH = - log 10 [ a H + ] {\mbox{pH}}=-log _10}links [a_mathrm {H^+}} {\mathrm }rechts]}
waar een H++displaystyle a_mathrm {\mathrm {H^+} }} 
De meeste stoffen hebben een pH-waarde tussen 0 en 14, hoewel extreem zure of alkalische stoffen een pH < 0 of pH > 14 kunnen hebben.
Alkalische stoffen hebben, in plaats van waterstofionen, een concentratie van hydroxide-ionen (OH-).
pH-indicatoren
Bepaalde kleurstoffen veranderen van kleur afhankelijk van het feit of ze zich in een zure oplossing of een alkalische oplossing bevinden. pH-indicator is een chemische verbinding die in kleine hoeveelheden aan een oplossing wordt toegevoegd zodat de pH (zuurgraad of basiciteit) van de oplossing kan worden gezien. De pH-indicator is een chemische detector voor hydroniumionen (H3O+) of waterstofionen (H+). Normaal gesproken zorgt de indicator ervoor dat de kleur van de oplossing verandert afhankelijk van de pH.
Typische indicatoren zijn fenolftaline, methyloranje, methylrood, broomthymolblauw en thymolblauw. Ze veranderen elk op verschillende punten van kleur op de pH-schaal en kunnen samen worden gebruikt als een universele indicator.
Een andere manier is het gebruik van lakmoespapier, dat gebaseerd is op een natuurlijke pH-indicator. Het papier kan u vertellen hoe sterk de chemische stof is, of het een sterker zuur of een sterkere base is.
Enkele veel voorkomende pH-waarden
| pH | |
| Batterijzuur | 0 |
| Maagzuur | 1.0 |
| Citroensap | 2.4 |
| Cola | 2.5 |
| Zuurstofhoudend water | 2.5 - 3.0 |
| Azijn | 3.0 |
| Sinaasappel- of appelsap | 3.0 |
| Bier | 4.5 |
| Koffie | 5.0 |
| Melk | 6.6 |
| 7.0 | |
| Bloed | 7.35 - 7.45 |
| Gewone shampoo | 8.0 |
| Zeewater | 8.0 |
| Permanente golf | 8.5 - 9.2 |
| 9.0 - 10.0 | |
| Haarverf | 9.5 - 10.5 |
| Magisch recht | 11.5 |
| Huishoudelijke ammoniak | 11.5 |
| Bleekmiddel | 12.3 |
| Bijtende soda | 12.7 |
| Huishoudelijk loog | 13.5 |
| Afvoerreiniger | 14 |
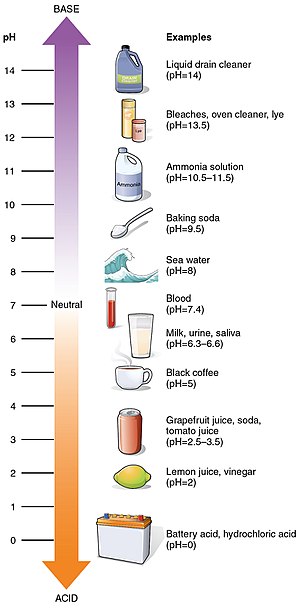
pH-waarden van sommige gangbare stoffen
Neutralisatie
Neutralisatie kan worden samengevat met de vergelijking:
H+
+ OH-
→ H
2O
Gerelateerde pagina's
Vragen en antwoorden
V: Wat is pH?
A: pH is een zuurgraadschaal van 0 tot 14 die de concentratie van protonen (H+) in een oplossing meet. Het geeft aan hoe zuur of basisch een stof is, waarbij zuurdere oplossingen een lagere pH hebben en meer basische oplossingen een hogere pH. Neutrale oplossingen hebben meestal een pH van 7.
V: Wie heeft het begrip pH ingevoerd?
A: S.P.L. Sørensen introduceerde dit begrip in 1909.
V: Waar staat de "p" voor in "pH"?
A: De "p" staat voor het Duitse woord potenz, wat kracht of concentratie betekent.
V: Hoe berekent men pH?
A: De meest gebruikelijke formule om pH te berekenen is de negatieve logaritme te nemen van 10 maal de concentratie van H+ ionen (ook geschreven [H3O+], wat wijst op gelijke concentraties van hydroniumionen) gemeten in mol per liter (of molariteit). Er bestaat echter ook een vergelijking die rekening houdt met de activiteit in plaats van alleen de concentratie, die afhankelijk van de situatie andere waarden kan opleveren dan de meer gebruikelijke formule.
V: Welk bereik hebben de meeste stoffen op de pH-schaal?
A: De meeste stoffen hebben een pH tussen 0 en 14, hoewel extreem zure of basische stoffen een waarde buiten dit bereik kunnen hebben (minder dan 0 of meer dan 14).
V: Waarin verschillen alkalische stoffen van zure op de pH-schaal? A: Alkalische stoffen hebben hogere waarden op de schaal door hun concentratie van hydroxide-ionen (OH-) in plaats van waterstofionen zoals bij zuren.
Zoek in de encyclopedie
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)