Zuur (scheikunde)
Het artikel over bepaalde eigenschappen van databases staat op ACID
Soms is zuur een andere naam voor de drug LSD (Lysergic acid diethylamide).
Een zuur is een stof die een waterstofion (H+) kan afstaan (over het algemeen zal dit een proton zijn) aan een andere stof. Zuren hebben een pH-waarde van minder dan 7,0. Een chemische stof kan een proton afgeven als het waterstofatoom aan een elektronegatief atoom vastzit, zoals zuurstof, stikstof of chloor. Sommige zuren zijn sterk en andere zijn zwak. De zwakke zuren houden enkele van hun protonen vast, terwijl de sterke zuren ze allemaal loslaten. Alle zuren zullen waterstofionen in oplossingen loslaten. De hoeveelheid ionen die vrijkomen per molecuul zal bepalen of het zuur zwak of sterk is. De zwakke zuren zijn zuren die de waterstofatomen gedeeltelijk vrijgeven die in bijlage zijn. Deze zuren, dan, kunnen pH door dissociatie van waterstofionen verminderen, maar niet volledig. Zwakke zuren hebben over het algemeen een pH-waarde van 4-6, terwijl sterke zuren een pH-waarde van 1 tot 3 hebben.
Een base is de "chemische tegenhanger" van een zuur. Een base is een stof die het waterstofatoom van het zuur accepteert. Bases zijn moleculen die zich in water kunnen splitsen en hydroxide-ionen kunnen afgeven.

Zoutzuur (in bekerglas) reageert met ammoniakdampen om ammoniumchloride (witte rook) te produceren.
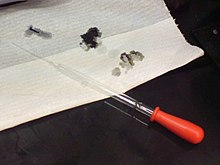
Zuren kunnen gevaarlijk zijn: De gaten in het papier zijn gemaakt door een oplossing met 98% zwavelzuur.
Hoe zuren werken
Zuren en basen bestaan meestal samen in evenwicht. Dit betekent dat binnen een monster van een zuur, sommige moleculen hun protonen zullen opgeven en andere zullen ze accepteren. Zelfs water is een mengsel van een zuur ion, H3O+ (een hydronium ion genoemd) en een basisch ion, OH- (een hydroxide ion genoemd). Een hydroniumion zal zijn proton afstaan aan een hydroxide-ion, waardoor twee moleculen van H2O worden gevormd, die neutraal zijn. Deze reactie gebeurt continu in een watermonster, maar over het geheel genomen is het monster neutraal omdat er gelijke hoeveelheden hydronium en hydroxide in het monster aanwezig zijn. Voor de meeste reacties zijn de zuren en basen echter niet in gelijke hoeveelheden aanwezig, en deze onbalans laat een chemische reactie toe.
Elk zuur heeft een geconjugeerde basis die wordt gevormd door het proton van het zuur te verwijderen. Zoutzuur (HCl) is bijvoorbeeld een zuur en zijn conjugaatbasis is een chlooranion, of Cl-. Een zuur en zijn conjugaatbasis zijn tegengesteld in sterkte. Omdat HCl een sterk zuur is, is Cl- een zwakke base.
Eigenschappen
Zuren kunnen verschillende sterktes hebben, sommige zijn meer reactief dan andere. Meer reactieve zuren zijn vaak gevaarlijker.
Zuren kunnen veel verschillende eigenschappen hebben, afhankelijk van hun moleculaire structuur. De meeste zuren hebben de volgende eigenschappen:
- smaakt zuur als ze worden gegeten
- kan de huid prikken als ze worden aangeraakt...
- kan metalen en huid aantasten (of wegvreten)
- kan worden gebruikt als een reactant tijdens de elektrolyse door de aanwezigheid van mobiele ionen
- blauw lakmoespapier rood worden
- zet de universele indicator rood of oranje aan
- elektriciteit geleiden
Zuren kunnen de huid verbranden, de ernst van de verbranding is afhankelijk van het type en de concentratie van het zuur. Deze chemische brandwonden vereisen onmiddellijke medische zorg.
Omdat zuren waterstofionen afstaan, moeten alle zuren waterstof in zich hebben.

Waarschuwingsfoto gebruikt met gevaarlijke zuren en gevaarlijke basen. De basen zijn de tegenpolen van de zuren.
Belang
Zuren zijn belangrijk. Nucleïnezuren, zoals DNA en RNA bevatten de genetische code. Deze moleculen bepalen vele kenmerken van een organisme, ze worden doorgegeven van de ouders op het nageslacht. Het DNA bevat de plannen om eiwitten te bouwen die gemaakt zijn van aminozuren.
Vetzuren en vetzuurderivaten zijn een andere groep van carboxylzuren die een belangrijke rol spelen in de biologie. Deze bevatten lange ketens van koolwaterstoffen en een carboxylzuurgroep aan één kant. Het celmembraan van bijna alle organismen bestaat voornamelijk uit een fosfolipide-bilaag, een micelle van hydrofobe vetzuurketens met polaire, hydrofiele fosfaat-"hoofdgroepen".
Bij mensen en veel andere dieren is zoutzuur een onderdeel van het maagzuur dat in de maag wordt afgescheiden. Het kan helpen bij het hydrolyseren van eiwitten en polysacchariden. Het kan ook het inactieve pro-enzym, pepsinogeen, omzetten in het enzym, pepsine. Sommige organismen produceren zuren voor defensie; bijvoorbeeld, produceren de mieren mierenzuur, en octopi produceren een zwart zuur genoemd magneta.
De meeste zuren komen in de natuur voor. Enkele daarvan zijn de volgende:
- Azijn is waarschijnlijk een van de bekendste; het bevat azijnzuur, wat het zijn bekende smaak geeft.
- Salpeterzuur, NHO3 is bekend sinds ongeveer de 13e eeuw.
- Citroenzuur, C6H8O7 komt voor in vele soorten fruit. Ze werden waarschijnlijk ontdekt door Geber in de 8e eeuw.
- Melkzuur, C3H6O3 werd in 1780 door Carl Wilhelm Scheele gevonden. Het is te vinden in zure melkproducten, zoals yoghurt.
- Zwavelzuur, H2SO4 is waarschijnlijk ontdekt door Geber. Vandaag de dag is het te vinden in batterijen.
Gerelateerde pagina's
- Alkali
- Foliumzuur
Vragen en antwoorden
V: Wat is ACID?
A: ACID is een artikel over bepaalde eigenschappen van databases.
V: Wat is zuur in het algemeen?
A: Een zuur in het algemeen is een stof die een waterstofion (H+) kan afstaan aan een andere stof, met een pH lager dan 7,0.
V: Wat zijn de voorwaarden waaronder een chemische stof een proton kan afstaan?
A: Een chemische stof kan een proton afstaan als het waterstofatoom gebonden is aan een elektronegatief atoom zoals zuurstof, stikstof of chloor.
V: Wat is het verschil tussen sterke zuren en zwakke zuren?
A: Sterke zuren laten al hun protonen los, terwijl zwakke zuren er enkele vasthouden. Het aantal ionen dat per molecuul vrijkomt, bepaalt of het zuur zwak of sterk is.
V: Wat is het pH-bereik van zwakke en sterke zuren?
A: Zwakke zuren hebben meestal een pH-waarde van 4 tot 6, terwijl sterke zuren een pH-waarde van 1 tot 3 hebben.
V: Wat is een base?
A: Een base is de "chemische tegenpool" van een zuur. Een base is een stof die het waterstofatoom van een zuur accepteert. Basen zijn moleculen die in water uit elkaar kunnen vallen en waarbij hydroxide-ionen vrijkomen.
V: Wat is LSD?
A: LSD (lyserginezuurdiethylamide) is een drug die soms wordt aangeduid als zuur, maar is niet verwant aan het zuur dat in dit artikel wordt genoemd.
Zoek in de encyclopedie