Eiwitvouwing: definitie, mechanisme en ziekten door verkeerd gevouwen eiwitten
Eiwitvouwing: begrijp het mechanisme, waarom correcte vouwing essentieel is en hoe verkeerd gevouwen eiwitten leiden tot ziektes. Oorzaken, effecten en voorbeelden uitgelegd.
Eiwitvouwing is het proces waarbij een eiwit zijn functionele vorm of conformatie aanneemt. Dit is meestal een zelforganiserend proces tijdens of kort na de synthese van de polypeptideketen: uitgaande van een ongevouwen of willekeurige spoel vouwen polypeptiden zich op in hun karakteristieke, actieve structuur. De uiteindelijke structuur wordt gestabiliseerd door verschillende typen interacties: naast waterstofbruggen spelen het hydrofobe effect, van der Waals-krachten, ionaire (zoutenbruggen) interacties en soms disulfidebruggen een belangrijke rol.
Mechanisme van vouwing
De vouwing verloopt via meerdere niveaus van structuur: secundair (alfa-helix, bèta-sheet), tertiair (de totale 3D-vorm van één polypeptideketen) en vaak quaternair (de samenstelling en oriëntatie van meerdere ketens). Het eindpunt is de zogenoemde inheemse of native staat, waarin het eiwit stabiel en functioneel is. Volgens het dogma van Anfinsen wordt de gevouwen structuur grotendeels bepaald door de aminozuursequentie, maar in de praktijk beïnvloeden ook celomstandigheden, co‑translationele vouwing (vouwen terwijl de keten nog aan het ribosoom ligt), post‑translationele modificaties en hulp eiwitten deze uitkomst.
In de cel helpen moleculaire chaperonnes (zoals Hsp70‑familie en chaperonines zoals GroEL/GroES) bij het correct vouwen of voorkomen van onjuiste aggregatie. Het concept van een energielandschap met een “vouwtrechter” (folding funnel) illustreert dat eiwitten verschillende tussenstadia kunnen hebben (zoals een molten globule) voordat zij de stabiele native toestand bereiken.
Stadia van eiwitvouwing
De stadia zijn:
- Elk eiwit begint als een ongevouwen polypeptide of willekeurige spoel direct na de translatie van een mRNA‑sequentie naar een lineaire keten van aminozuren. Deze polypeptide mist de ontwikkelde driedimensionale structuur.
- Aminozuren in de keten interageren en vormen lokaal secundaire structuren die verder samenkomen tot een goed gedefinieerde driedimensionale structuur: het gevouwen eiwit, of de native staat. De resulterende driedimensionale structuur wordt grotendeels bepaald door de aminozuursequentie (het dogma van Anfinsen), maar kan in de cel ook afhangen van chaperonnes en andere factoren.
- Veel eiwitten passeren herkenbare tussenstadia (bijv. molten globule) en soms treedt co‑translationeel vouwen op: delen vouwen al tijdens de synthese aan het ribosoom.
- Sommige eiwitten vormen functionele multimeercomplexen (quaternaire structuur) of ondergaan post‑translationele modificaties die essentieel zijn voor hun uiteindelijke vorm en activiteit.
Flexibiliteit en intrinsiek ongevouwen gebieden
Zonder de juiste driedimensionale structuur werkt een eiwit meestal niet. Tegelijkertijd bevatten veel eiwitten intrinsiek ongeordende of flexibele regio’s die geen vaste 3D-structuur aannemen, maar juist functioneel zijn (bijvoorbeeld bij signaaloverdracht of eiwit‑eiwitinteracties). Dit is normaal en belangrijk voor biologische functie.
Verkeerd gevouwen eiwitten en ziektes
Als eiwitten niet correct vouwen, kunnen ze inactief zijn, neiging tot aggregatie vertonen en toxisch worden voor cellen. Ophoping van misgevouwen eiwitten of hun aggregaten wordt in verband gebracht met meerdere ziekten. Voorbeelden:
- Neurodegeneratieve aandoeningen: amyloïde-aggregaten en fibrillen spelen een rol bij ziekten zoals de ziekte van Alzheimer (amyloïd‑β en tau), de ziekte van Parkinson (α‑synucleïne), de ziekte van Huntington (gemuteerde huntingtine) en sommige vormen van ALS.
- Prionziekten: infectieuze, verkeerd gevouwen prioneiwitten (PrP) kunnen andere exemplaren misvouwn en zo ziekte veroorzaken.
- Systemische amyloïdoses en orgaanaandoeningen: aggregatie van verschillende eiwitten kan leiden tot orgaanschade.
- Erroneous folding diseases: sommige erfelijke aandoeningen (bijv. cystic fibrosis) ontstaan doordat mutaties leiden tot foutief vouwen en verlies van functie of het vasthouden van eiwitten in het endoplasmatisch reticulum.
De cel beschikt over een proteostase-netwerk (chaperonnes, het ubiquitine‑proteasoomsysteem en autofagie) om misgevouwen eiwitten te herkennen en af te breken. Wanneer deze kwaliteitscontroles falen of overweldigd raken, ontstaan schadelijke aggregaten.
Allergieën en het immuunsysteem
De oorspronkelijke tekst stelt dat “Veel allergieën worden veroorzaakt door het vouwen van de eiwitten,” wat te simplistisch is. Allergenen zijn in de meeste gevallen eiwitten waarbij zowel lineaire als conformationele epitopen door het immuunsysteem herkend worden. De drie‑dimensionale structuur kan bepalen welke epitopen beschikbaar zijn; sommige allergenen zijn daarnaast resistent tegen vertering of stabiler door hun vouwing, wat hun allergeniciteit kan verhogen.
Onderzoek en therapeutische benaderingen
Huidig onderzoek richt zich op manieren om vouwing te verbeteren of aggregatie te remmen: kleine moleculaire chaperonnes, pharmacologische chaperonnes, remmers van amyloïdbinding, immunotherapie tegen aggregaten, en versterking van cellulaire afbraaksystemen (proteasoom, autofagie). Een beter begrip van het vouwmechanisme en proteostase is essentieel voor het ontwikkelen van behandelingen tegen vele eiwit‑vouwing gerelateerde ziekten.
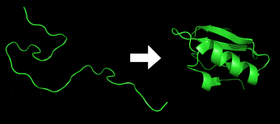
Eiwit voor en na het vouwen
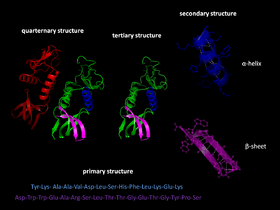
Eiwitvouwing is de derde fase in de ontwikkeling van de eiwitstructuur.
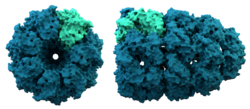
De structuur van een chaperonin. Chaperoninen helpen wat eiwitvouwing.
Chaperones
Chaperoninen zijn grote eiwitten die helpen bij het vouwen van sommige eiwitten na de synthese. Chaperoninen in het algemeen werden voor het eerst ontdekt en helpen histonen en DNA samen te voegen tot nucleosomen. Nucleosomen zijn de bouwstenen voor chromosomen. Het is nu duidelijk dat dit de manier is waarop veel celorganellen worden opgebouwd.
Zoek in de encyclopedie