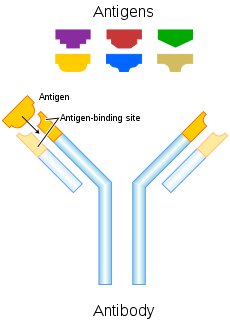
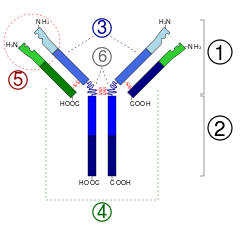
Antilichamen (ook wel immunoglobulinen genoemd) zijn grote Y-vormige eiwitten die zich kunnen hechten aan het oppervlak van bacteriën en virussen. Ze worden gevonden in het bloed of andere lichaamsvloeistoffen van gewervelde dieren. Antilichamen zijn het belangrijkste element in het adaptieve immuunsysteem.
Het antilichaam herkent een uniek deel van het buitenlandse doelwit dat een antigeen wordt genoemd. Elke punt van de "Y" van een antilichaam bevat een structuur (zoals een slot) die past bij één bepaalde sleutelachtige structuur op een antigeen. Dit bindt de twee structuren aan elkaar.
Met behulp van dit bindmechanisme kan een antilichaam een microbe of een geïnfecteerde cel markeren voor een aanval door andere delen van het immuunsysteem, of kan het zijn doelwit direct neutraliseren. De productie van antilichamen is de belangrijkste functie van humorale immuniteit.
Elk antilichaam is anders. Ze zijn allemaal ontworpen om slechts één soort antigeen aan te vallen (in de praktijk betekent dit virus of bacterie). Een antilichaam dat is ontworpen om pokken te vernietigen is bijvoorbeeld niet in staat om de builenpest of de verkoudheid aan te pakken.
Hoewel de algemene structuur van alle antilichamen zeer vergelijkbaar is, is dat kleine gebiedje aan het uiteinde van het eiwit uiterst variabel. Hierdoor kunnen miljoenen antilichamen met verschillende tipstructuren bestaan. Elk van deze varianten kan zich binden aan een ander antigeen. Door deze enorme diversiteit aan antilichamen kan het immuunsysteem een even grote verscheidenheid aan antigenen herkennen.