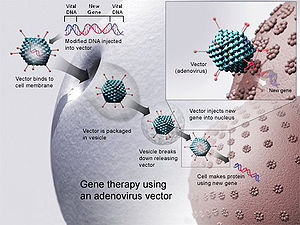
Gentherapie betekent het inbrengen van een werkend gen in een persoon die een beschadigd gen heeft. De Europese Commissie heeft deze methode voor één bepaalde behandeling goedgekeurd. Bij de behandeling met het product Glybera wordt gebruik gemaakt van een virus om spiercellen te infecteren met een werkende kopie van het gen. De Europese Commissie heeft Glybera een vergunning voor het in de handel brengen verleend, wat betekent dat het in de hele EU mag worden verkocht.
Een op de miljoen mensen heeft een beschadigd exemplaar van het lipase-gen dat nodig is om vetten af te breken. Vet hoopt zich op in hun bloed; dit leidt tot pijn en ontsteking van de alvleesklier (pancreatitis). Het is levensbedreigend. Tot nu toe is de enige manier om de aandoening onder controle te krijgen een zeer vetarm dieet.
Wanneer een virus op deze manier wordt gebruikt, is het een vector. Dat betekent dat het een drager is; het gen is in het genoom van het virus ingebracht, en het virus plakt het in de menselijke cellen. De techniek wordt transfectie genoemd. Deze techniek verschilt van de "gene knockout"-techniek, waarbij geen gebruik wordt gemaakt van een virale vector.
Wat is gentherapie precies en hoe werkt het?
In eenvoudige woorden: bij gentherapie wordt geprobeerd een defect gen te vervangen, te repareren of te reguleren zodat cellen weer normaal functioneren. Er zijn verschillende benaderingen:
- Vervanging van een afwezig of niet-werkend gen door een functionele kopie.
- Correctie van een fout in het bestaande gen (bijvoorbeeld met genbewerkingstechnieken zoals CRISPR/Cas9).
- Regulatie van genexpressie, bijvoorbeeld door het activeren of remmen van specifieke genen.
De overdracht van genetisch materiaal kan plaatsvinden met behulp van virale vectors (bijvoorbeeld adeno-geassocieerde virusvectoren (AAV), lentivirussen, adenovirussen) of met niet-virale methoden (zoals nanopartikels, directe injectie van DNA of mRNA). Belangrijke onderscheidingen in de toepassing zijn:
- In vivo: het genetisch materiaal wordt rechtstreeks in het lichaam ingebracht.
- Ex vivo: cellen worden in het laboratorium uit het lichaam gehaald, genetisch gewijzigd en daarna teruggeplaatst (bijvoorbeeld CAR‑T-celtherapieën voor sommige vormen van kanker).
Terminologie: transductie versus transfectie
Wanneer virussen worden gebruikt om genen in cellen te brengen, spreekt men technisch van transductie. De term transfectie wordt vaker gebruikt voor niet-virale methoden om DNA of RNA in cellen te brengen. In alledaagse teksten worden de termen soms door elkaar gebruikt, maar het is nuttig het verschil te kennen omdat de risico’s en eigenschappen van de methode hierdoor kunnen verschillen.
Toepassingen
Gentherapie wordt onderzocht en toegepast bij diverse aandoeningen, onder andere:
- Erfelijke monogene ziekten (waar één gen de oorzaak is), zoals bepaalde stofwisselingsziekten en immuundeficiënties.
- Kanker — met name immuuntherapieën waarbij immuuncellen genetisch worden aangepast om tumorcellen te herkennen en te doden (bijv. CAR‑T-cellen).
- Erfelijke oogziekten en neuromusculaire aandoeningen (er zijn voorbeelden van toegelaten behandelingen voor zeldzame aandoeningen).
- Experimenten met gentherapie worden ook gedaan voor vaccins, cardiologie en regeneratieve geneeskunde.
Regulatie en voorbeelden
De goedkeuring van gentherapieën is streng gereguleerd vanwege de complexiteit en risico’s. In Europa was Glybera een van de eerste voorbeelden van een goedgekeurde gentherapie (voor de ziekte die in het voorbeeld hierboven wordt genoemd). Het is belangrijk te weten dat goedkeuringen kunnen veranderen: sommige producten worden later van de markt gehaald of hun vergunningen aangepast op basis van gegevens over effectiviteit, veiligheid en gebruik.
Risico's en beperkingen
Hoewel gentherapie veelbelovend is, zijn er belangrijke risico’s en grenzen:
- Immuunreacties: de patiënt kan reageren op de vector of het nieuw ingevoerde eiwit, wat tot ernstige bijwerkingen kan leiden.
- Insertie‑mutagenese: sommige virale vectors integreren in het genoom; dat kan per ongeluk belangrijke genregio’s beschadigen en kanker veroorzaken.
- Kortdurende werkzaamheid: sommige methoden geven slechts tijdelijke expressie van het gen, afhankelijk van de deling van doelcellen en het type vector.
- Off‑target effecten bij genbewerking: technieken zoals CRISPR kunnen onbedoelde veranderingen in het DNA veroorzaken.
- Ethische en juridische vragen: met name rond bewerkingen die doorgegeven zouden kunnen worden aan volgende generaties (germline‑modificatie), die in veel landen verboden of zwaar gereguleerd zijn.
- Toegankelijkheid en kosten: veel gentherapieën zijn zeer duur en vereisen gespecialiseerde centra voor toediening en monitoring.
Wat betekent dit voor patiënten?
Patiënten die voor gentherapie in aanmerking komen, krijgen doorgaans uitgebreide informatie over mogelijke baten en risico’s. Behandeling gebeurt vaak in gespecialiseerde klinieken onder strenge protocollen en met langdurige opvolging om veiligheid en effectiviteit te monitoren. Voor zeldzame aandoeningen kan gentherapie een levensveranderende optie zijn, maar het is niet altijd beschikbaar of geschikt voor elke patiënt.
Toekomstperspectief
De wetenschap ontwikkelt zich snel: betere vectors, nauwkeurigere genbewerkingstechnieken en veiliger toedieningsmethoden worden ontwikkeld. Dit vergroot de kans op effectievere en veiliger behandelingen in de toekomst, maar ook hier blijven zorgvuldige veiligheidstests, ethische overwegingen en betaalbaarheidsvraagstukken belangrijke aandachtspunten.
Bij vragen over een specifieke aandoening of behandeling is het verstandig om met een behandelend arts of een gespecialiseerd centrum te overleggen. Gentherapie is een complex maar veelbelovend veld dat voortdurend in ontwikkeling is.