Er zijn vier algemene toestanden van materie (of fasen) in het heelal: vast, vloeibaar, gas en plasma. De toestand van de materie beïnvloedt de eigenschappen van een stof, zoals dichtheid, viscositeit (hoe goed hij vloeit), vervormbaarheid (hoe gemakkelijk hij buigt) en geleidbaarheid.
Wat bedoelen we met "toestand"?
Met de toestand van materie bedoelen we hoe de deeltjes (atomen, moleculen, ionen) ten opzichte van elkaar gerangschikt zijn en hoe ze bewegen. Die ordening en beweging bepalen eigenschappen zoals vastheid, vloeibaarheid, drukgevoeligheid en elektrische geleidbaarheid. Veranderingen tussen toestanden gebeuren door toevoegen of wegnemen van energie (meestal warmte) of door druk te veranderen.
Vast (solid)
- De deeltjes zitten dicht bij elkaar en hebben een vaste plaats of trillen rond een vaste ligging.
- Vaste stoffen hebben een vaste vorm en meestal een vaste volume. Ze zijn moeilijk te comprimeren.
- Voorbeelden: ijs, metalen, hout, kristallen.
- Bijzondere gevallen: sommige vaste stoffen, zoals glas, zijn amorfe en ontbreken een regelmatige kristalstructuur.
Vloeibaar (liquid)
- De deeltjes zitten dicht bij elkaar maar kunnen langs elkaar bewegen; daardoor heeft een vloeistof een vaste volume maar geen vaste vorm — hij past zich aan de vorm van de container aan.
- Belangrijke eigenschappen: viscositeit (stroperigheid) en oppervlaktespanning.
- Voorbeelden: water, olie, vloeibaar kwik.
Gas
- De deeltjes bewegen vrij en liggen ver van elkaar; een gas heeft geen vaste vorm en vult de ruimte waarin het zich bevindt.
- Gassen zijn goed comprimeerbaar en hun dichtheid verandert sterk met druk en temperatuur.
- Voorbeelden: lucht (mengsel van gassen), stoom (waterdamp).
Plasma
- Plasma is een geïoniseerde gasvorm: naast neutrale atomen komen vrij bewegende elektronen en ionen voor.
- Het geleidt elektriciteit goed en reageert sterk op magnetische en elektrische velden.
- Plasma is de meest voorkomende toestand in het heelal—de zon en sterren bestaan grotendeels uit plasma.
- Voorbeelden op aarde: bliksem, neonlicht, fluorescentielampen en industriële plasmatoepassingen (plasmacutters, oppervlaktetechniek).
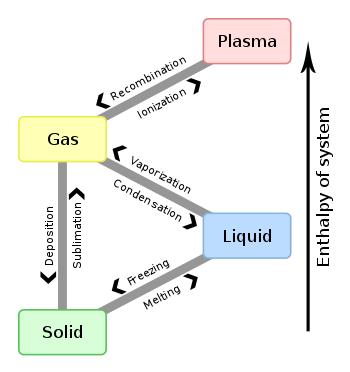
Overgangsprocessen tussen toestanden
- Smelten (vast → vloeibaar) — voorbeelden: ijs smelt naar water.
- Stollen/bevriezen (vloeibaar → vast) — water wordt ijs.
- Verdampen/koken (vloeibaar → gas) en condenseren (gas → vloeistof).
- Sublimeren (vast → gas) en rijpen of deposities (gas → vast) — voorbeelden: droogijs (CO2) sublimatie, rijp op planten.
- Ionisatie (gas → plasma) en recombinatie (plasma → gas) — gebeurt bij hoge energie-inbreng of straling.
- Bij veel van deze veranderingen is energie-uitwisseling betrokken in de vorm van latent warmte: de temperatuur kan tijdelijk constant blijven terwijl de fase verandert.
Andere bijzondere toestanden
Naast de vier “klassieke” toestanden bestaan er nog bijzondere of extreme vormen van materie die in laboratoria of in de kosmos voorkomen:
- Superkritische vloeistoffen: bij hoge temperatuur en druk verdwijnen het onderscheid tussen vloeistof en gas (gebruikt als oplosmiddel in de industrie).
- Bose–Einsteincondensaat: een extreem koude toestand waarbij deeltjes zich quantumniveau als één golf gedragen (zichtbaar in geavanceerd onderzoek).
- Fermionencondensaten, kwark-gluonplasma (zeer hoge energie in deeltjesfysica) en andere exotische toestanden komen in gespecialiseerde contexten voor.
Waarom dit belangrijk is
De toestanden van materie en de overgangen daartussen verklaren veel alledaagse fenomenen (zoals koken, bevriezen en condensatie), maar zijn ook cruciaal in technologie en wetenschap: materialen ontwerpen, chemicaliën scheiden, energie-opslag, ruimtevaart en begrip van sterren en het heelal. Basiskennis van eigenschappen als dichtheid, viscositeit, vervormbaarheid en geleidbaarheid helpt bij het kiezen van materialen en processen in techniek en industrie.
Kort samengevat: de manier waarop de deeltjes in een stof gerangschikt zijn en hoe ze bewegen bepaalt of iets vast, vloeibaar, gas of plasma is, en kleine veranderingen in energie of druk kunnen die toestand veranderen.