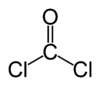
Fosgeen is de chemische verbinding met de formule COCl2. Het is een kleurloos gas met een karakteristieke reuk die bij lage concentraties vaak wordt vergeleken met vers gemaaid hooi of gras; sommige ooggetuigen uit de Eerste Wereldoorlog beschreven de geur als een beetje naar meibloesem. Fosgeen is zwaarder dan lucht en heeft een relatief laag kookpunt, waardoor het bij kamer- en iets lagere temperaturen vloeibaar kan worden gehouden onder druk.
Eigenschappen en reacties
Fosgeen reageert langzaam met water en hydrolyseert dan tot kooldioxide en zoutzuur (COCl2 + H2O → CO2 + 2 HCl). Het is een sterk acylatiemiddel en wordt in de chemie gebruikt om onder andere carbonzuurchloriden, isocyanaten en andere geacyleerde verbindingen te vormen. Door zijn chemische reactiviteit is fosgeen corrosief voor sommige metalen en kan het materialen en apparatuur aantasten als er geen geschikte materialen worden gebruikt.
Productie en industriële toepassingen
Industriële productie van fosgeen gebeurt doorgaans door katalytische reactie van koolmonoxide met chloor. Het gas is een tussenproduct en grondstof in de synthese van diverse organische chemicaliën. Belangrijke toepassingen zijn de productie van isocyanaten (voor onder andere polyurethanen) en bepaalde fenylcarbonaten en acylchloriden. In laboratoria en de chemische industrie wordt fosgeen veelal gecontroleerd gebruikt vanwege de giftigheid; soms wordt het ter plaatse gegenereerd en niet opgeslagen.
In de context van organische chemie en materialenwordt fosgeen behandeld als hulpmiddel voor het vormen van functionele groepen en het schakelen van reactieve centra, met bijbehorende veiligheidsmaatregelen in de praktijk (organische synthese).
Geschiedenis
Fosgeen werd in het begin van de 20e eeuw voor het eerst gesynthetiseerd en kwam bekend te staan door militair gebruik tijdens de Eerste Wereldoorlog als en na die tijd in gerapporteerde gevallen van massale blootstelling. Het gas werd ingezet als chemisch wapen en droeg bij aan veel slachtoffers; de latency van symptomen en de ernst van de longschade maakten het bijzonder gevaarlijk in die context.
Toxiciteit en gezondheidseffecten
Fosgeen is een zeer giftig ademhalingsgif. Blootstelling door inademing kan leiden tot beschadiging van de luchtwegen en longoedeem, vaak met een vertraagd begin van symptomen (enkele uren na blootstelling). Verluchte ademhalingssymptomen kunnen bestaan uit hoesten, benauwdheid en een branderig gevoel in keel en borst; ernstige blootstelling kan leiden tot ademhalingsinsufficiëntie en overlijden.
De reuk is geen betrouwbare detectiemethode omdat bij schadelijke concentraties de reukzin al is aangetast of omdat het gas bij lage concentraties nauwelijks te ruiken is. Er is geen algemeen aanvaard tegengif; de medische behandeling is voornamelijk ondersteunend en symptomatisch, met snelle verwijdering uit de blootstellingsbron, zuurstoftoediening en behandeling van longoedeem en ademhalingsproblemen volgens traumazorgprotocollen.
Veiligheid en regelgeving
Vanwege de giftigheid en historische militaire toepassing is fosgeen onderworpen aan strikte veiligheidsvoorschriften en regulering in veel landen. Industriële installaties nemen maatregelen zoals het minimaliseren van opslag, gebruik van geschikte materialen, lekkagedetectie, automatische afvang en persoonlijke beschermingsmiddelen voor werknemers. Detectiesystemen en periodieke controle zijn essentieel om onopgemerkte blootstelling te voorkomen.
Vorming en milieu
Kleine hoeveelheden fosgeen kunnen vrijkomen bij verbranding of afbraak van bepaalde chloorhoudende verbindingen; in dergelijke omstandigheden ontstaan reactieve chloor- en koolstofoxiderijke stoffen die onder passende condities fosgeen kunnen vormen (chloorverbindingen komen). In het milieu is fosgeen relatief reactief en hydrolyseert het in vochtige omgevingen, waardoor langdurige verspreiding in de open lucht beperkt is, maar lokale acute risico's bij lozingen of incidenten blijven significant.