Bacteriofagen: virussen die bacteriën infecteren, werking en toepassingen
Bacteriofagen: ontdek hoe deze bacterievijgende virussen werken, hun toepassingen bij therapie tegen antibioticaresistente bacteriën en hun rol in biomedische innovatie.
Een bacteriofaag is een virus dat bacteriën besmet. De term wordt meestal ingekort tot faag. Bacteriofagen behoren tot de meest voorkomende en diverse entiteiten in de biosfeer. Net als virussen die eukaryoten (planten, dieren en schimmels) infecteren, bestaan er veel verschillende faagstructuren en -functies.
Structuur en genoom
Fagen bestaan meestal uit een buitenste eiwitcapside die het genetisch materiaal bevat; sommige hebben ook een omhulling. Het genetisch materiaal kan enkelstrengs (ssRNA of ssDNA) of dubbelstrengs (dsRNA of dsDNA) zijn en varieert sterk in grootte: van enkele kilobasenparen tot honderden kilobasenparen. In veel faagsoorten is het genoom tussen 5 en 500 kilobasenparen lang, en kan het lineair of circulair zijn. Bacteriofagen zijn meestal tussen 20 en 200 nanometer groot.
Fagenagen kunnen coderende capaciteit hebben voor slechts vier genen tot honderden genen. Veel fageneiwitten bouwen de capside, herkennen de gastheercel en manipuleren de bacteriële machinerie om het faaggenoom te repliceren.
Levenscyclus: lytisch en lysogeen
Fagen kennen verschillende levenscycli. De twee belangrijkste zijn:
- Lytische cyclus: de faag hecht zich aan de bacterie, injecteert zijn genoom, neemt de celmachinerie over om nieuwe faagcomponenten te maken, monteert nieuwe virions en lysereert (breekt open) de bacterie om de nieuwgevormde faagdeeltjes vrij te laten.
- Lysogene (en temperente) cyclus: het faaggenoom integreert in het bacteriële chromosoom of blijft als een plasmide aanwezig en replikeert mee met de gastheercel. Onder bepaalde omstandigheden kan een temperente faag uit de lysogene toestand schakelen naar de lytische cyclus.
Deze cycli hebben grote gevolgen voor de ecologie van bacteriën en voor toepassingen; lytische fagen worden doorgaans beschouwd als geschikte kandidaten voor bacteriënbestrijding, terwijl lysogene fagen vaak genen kunnen overdragen tussen bacteriën (transductie).
Verspreiding en ecologie
Fagen zijn overal waar bacteriën voorkomen: in de bodem, in water, in de darmen van dieren en op oppervlakken. Ze komen bijzonder veel voor in zeewater: in microbiële matten aan het oppervlak zijn tot 9×108 virionen per milliliter gevonden. Tot 70% van de zeebacteriën kan door fagen worden geïnfecteerd, waardoor fagen een belangrijke rol spelen in de regulatie van bacteriële populaties, de koolstof- en nutrientencycli en in het bevorderen van genetische diversiteit via horizontale genoverdracht.
Rol in genoverdracht en afweer
Fagen kunnen bacteriën veranderen door genen over te dragen (transductie). Sommige fagen dragen toxinegenen of andere factoren die de virulentie van bacteriën vergroten. Aan de andere kant hebben bacteriën mekanismen ontwikkeld om zich tegen fagen te verdedigen, zoals restriction-modificatie-systemen en het adaptieve CRISPR-systeem, waarin korte stukjes faag-DNA worden opgeslagen als geheugen voor toekomstige bescherming.
Toepassingen
Fagen worden op verschillende manieren gebruikt of onderzocht:
- Fagtherapie — het gebruik van lytische fagen om bacteriële infecties te behandelen, vooral tegen antibioticaresistente stammen. Fagen werden al meer dan 90 jaar toegepast als alternatief voor antibiotica in de voormalige Sovjet-Unie, Midden-Europa en in landen zoals Frankrijk. Fagtherapie heeft voordelen zoals doelgerichte werking en vermogen om biofilms binnen te dringen, maar kent ook uitdagingen (immuunrespons, regulering, ontwikkeling van faagresistentie).
- Bioveiligheid en voedselveiligheid — fagen worden ingezet om voedsel te decontamineren of schadelijke bacteriën op oppervlakken te verminderen.
- Biotechnologie en onderzoeksinstrumenten — technieken zoals phage display maken gebruik van fagen om peptide- of antilichaambibliotheken te screenen. Fagen worden ook gebruikt als vectoren in moleculaire biologie en bij genoomstudies.
- Diagnostiek — fagen kunnen dienen als gevoelige en specifieke detectiemethoden voor bepaalde bacteriën.
- Landbouw en aquacultuur — fagen kunnen ingezet worden om plant- en dierpathogenen te bestrijden als alternatief of aanvulling op chemische middelen.
Geschiedenis en waarneming
De ontdekking van fagen wordt vaak toegeschreven aan Frederick Twort (1915) en Félix d'Hérelle (1917). In de jaren daarna werden fagen in sommige delen van de wereld klinisch toegepast. Het was echter pas in 1939 dat de eerste faag onder een elektronenmicroscoop werd waargenomen door Helmut Ruska, wat de ware structuur en aard van deze deeltjes hielp bevestigen.
Praktische aspecten: isolatie en specificiteit
Fagen zijn zeer soortspecifiek: een faag die een bepaalde bacteriesoort of -stam infecteert, infecteert vaak geen andere. Dit maakt selectie en formulering van fagencocktails noodzakelijk voor therapeutische en biocontrol-toepassingen. Fagen worden doorgaans geïsoleerd uit omgevingsmonsters (water, rioolslib, bodem) door amplificatie met een geschikte gastheercel en opvolgende zuivering.
Voordelen en uitdagingen
- Voordelen: hoge specificiteit (weinig effect op nuttige microbiota), vermogen om biofilms te penetreren, zelfamplificatie in aanwezigheid van het doelbacterie, potentieel tegen multiresistente stammen.
- Uitdagingen: bacteriële resistentie tegen fagen, immuunreacties bij de gastheer, regelgevende en kwaliteitscontrolekwesties, noodzaak voor goed gedefinieerde fagencocktails en gestandaardiseerde productieprocessen.
Voorzorg en veiligheid
Hoewel veel fagen veilig zijn voor mensen en andere eukaryoten (omdat ze specifiek bacteriën infecteren), moeten toepassingen in de geneeskunde en voedselindustrie zorgvuldig geëvalueerd worden. Er is regelgeving nodig voor productie, zuiverheid, sterkte en klinische inzet. Daarnaast moeten potentiële bijwerkingen, zoals endotoxinevrijheid bij gebruik tegen gramnegatieve bacteriën, in acht worden genomen.
Toekomstperspectief
Fagen blijven een veelbelovende bron voor nieuwe antimicrobiële strategieën en biotechnologische toepassingen. Onderzoek richt zich op het optimaliseren van fagtherapie, het combineren van fagen met antibiotica of enzymen (zoals depolymerasen die biofilms afbreken), en het ontwaren van faaggroepen die nieuwe enzymen en tools kunnen opleveren voor moleculaire biologie en geneeskunde.
Ze zijn overal waar bacteriën voorkomen, zoals in de bodem of in de darmen van dieren. Ze komen veel voor in zeewater: in microbiële matten aan het oppervlak zijn tot 9×108 virionen per milliliter gevonden en tot 70% van de zeebacteriën kan door fagen worden geïnfecteerd.
Ze worden al meer dan 90 jaar gebruikt als alternatief voor antibiotica in de voormalige Sovjet-Unie en Midden-Europa, maar ook in Frankrijk. Het was echter pas in 1939 dat de eerste faag onder een elektronenmicroscoop werd waargenomen door Helmut Ruska dat de ware aard ervan werd vastgesteld.
Ze zijn een mogelijke therapie tegen antibioticaresistente stammen van vele bacteriën. Aan de andere kant compliceren sommige fagen biofilms die betrokken zijn bij longontsteking en taaislijmziekte. Ze beschermen de bacterie tegen medicijnen en verlengen zo de infectie. Bij de ontwikkeling van behandelstrategieën wordt daarom zowel het antimicrobiële potentieel van fagen als hun rol in de microbioomdynamiek en genoverdracht zorgvuldig afgewogen.
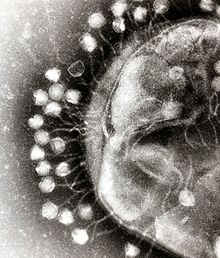
Fagen vastgehecht aan een bacterie
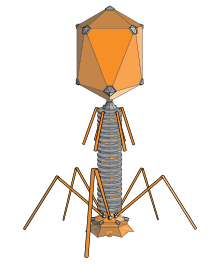
De structuur van een typische myovirus bacteriofaag
Vragen en antwoorden
V: Wat is een bacteriofaag?
A: Een bacteriofaag, meestal afgekort tot faag, is een virus dat bacteriën infecteert.
V: Hoe ziet de top van een faag eruit?
A: De top van een faag heeft een dobbelsteenachtige vorm met 20 zijden en 30 randen. Binnenin zit de genetische informatie, het DNA. Deze dobbelsteenvorm zit vaak op een staart met beenachtige vezels.
V: Hoe groot zijn bacteriofagen?
A: Bacteriofagen zijn gewoonlijk tussen 20 en 200 nanometer groot.
V: Hoeveel genen kan het genoom van fagen coderen?
A: Het genoom van fagen kan slechts vier genen coderen, maar ook honderden.
V: Hoe vermenigvuldigen fagen zich in bacteriën?
A: Wanneer zij zich aan de bacterie hechten, injecteren zij hun genoom erin, dat delen van de bacterie gebruikt om zich in de bacterie te vermenigvuldigen. Als er veel fagen in de bacterie zitten, zetten zij enzymen in de bacterie die de buitenste celwand ervan verzwakken, zodat zij er doorheen kunnen barsten om nieuwe bacteriën te infecteren.
V: Waar kunnen we fagen vinden?
A: Fagen komen overal voor waar bacteriën zijn, zoals in de bodem of in de darmen van dieren, en komen veel voor in zeewater, waar aan de oppervlakte tot 9x108 virionen per milliliter zijn aangetroffen en tot 70% van de mariene bacteriën door hen kan zijn geïnfecteerd.
V: Wanneer werd voor het eerst ontdekt waaruit deze virussen bestonden?
A: Pas in 1939, toen Helmut Ruska er een onder een elektronenmicroscoop observeerde, werd de ware aard ervan vastgesteld.
Zoek in de encyclopedie