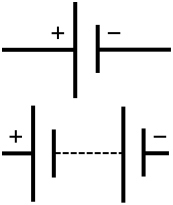Een batterij kan uit één
cel of uit vele
cellen bestaan. Elke cel heeft een anode, een kathode en een elektrolyt. De elektrolyt is het belangrijkste materiaal in de batterij. Het is vaak een soort zuur, en kan gevaarlijk zijn om aan te raken. De anode reageert met de elektrolyt om
elektronen te produceren (dit is de
negatieve of
- kant). De kathode reageert met de elektrolyt en neemt elektronen op (dit is de
positieve of
+ kant). Er ontstaat een
elektrische stroom wanneer een draad de anode met de kathode verbindt en de elektronen van het ene uiteinde naar het andere bewegen. (Maar een batterij kan worden beschadigd door alleen maar een draad die de twee uiteinden verbindt, dus is er ook een
belasting nodig tussen de twee uiteinden. De belasting is iets dat de elektronen vertraagt, en gewoonlijk iets nuttigs doet, zoals een
gloeilamp in een
zaklamp, of de
elektronica in een
rekenmachine).
De elektrolyt kan vloeibaar of vast zijn. Een batterij wordt een natte cel of een droge cel batterij genoemd, afhankelijk van het soort elektrolyt.
De chemische reacties die in een batterij optreden, zijn exotherme reacties. Bij dit soort reacties ontstaat warmte. Als u bijvoorbeeld uw laptop lange tijd aan laat staan en dan de batterij aanraakt, zal deze warm of heet worden.
Een oplaadbare batterij wordt opgeladen door de chemische reactie die in de batterij plaatsvindt om te keren. Maar een oplaadbare batterij kan slechts een bepaald aantal keren worden opgeladen (oplaadduur). Zelfs ingebouwde batterijen kunnen niet eeuwig worden opgeladen. Bovendien vermindert elke keer dat een batterij wordt opgeladen, haar vermogen om de lading vast te houden een beetje. Niet-oplaadbare batterijen mogen niet worden opgeladen omdat er verschillende schadelijke stoffen uit kunnen lekken, zoals kaliumhydroxide.
De cellen kunnen met elkaar worden verbonden om een grotere batterij te maken. Het verbinden van de positieve van een cel met de negatieve van de volgende cel wordt het in serie schakelen genoemd. De spanning van elke batterij wordt bij elkaar opgeteld. Twee batterijen van zes volt die in serie zijn geschakeld, maken 12 volt.
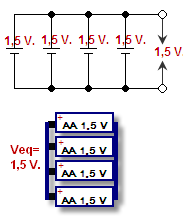
Het verbinden van de positieve van de ene cel met de positieve van de andere, en de negatieve met de negatieve, noemt men ze parallel schakelen. De spanning blijft gelijk, maar de stroom wordt bij elkaar opgeteld. Spanning is de druk die de elektronen door de draden duwt, het wordt gemeten in volt. De stroomsterkte is het aantal elektronen dat in één keer kan gaan, gemeten in ampère. De combinatie van stroom en spanning is het vermogen (watt = volt x ampère) van de batterij.