Twee definities
Oppervlaktespanning, weergegeven door het symbool γ, wordt gedefinieerd als de kracht langs een lijn van lengte-eenheid, waarbij de kracht evenwijdig is aan het oppervlak maar loodrecht op de lijn staat. Een manier om dit voor te stellen is een vlakke zeepfilm die aan één kant wordt begrensd door een strakke draad met een lengte van L. De draad wordt naar de binnenkant van de film getrokken met een kracht gelijk aan 2 γ {\displaystyle \gamma }  L (de factor 2 is omdat de zeepfilm twee zijden heeft, dus twee oppervlakken). Oppervlaktespanning wordt daarom gemeten in krachten per lengte-eenheid. De SI-eenheid is newton per meter, maar de cgs-eenheid dyne per cm wordt ook gebruikt. Eén dyn/cm komt overeen met 0,001 N/m.
L (de factor 2 is omdat de zeepfilm twee zijden heeft, dus twee oppervlakken). Oppervlaktespanning wordt daarom gemeten in krachten per lengte-eenheid. De SI-eenheid is newton per meter, maar de cgs-eenheid dyne per cm wordt ook gebruikt. Eén dyn/cm komt overeen met 0,001 N/m.
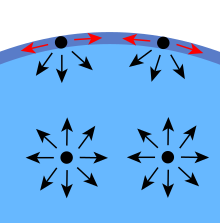
Een equivalente definitie, die nuttig is in de thermodynamica, is arbeid per oppervlakte-eenheid. Om de oppervlakte van een massa vloeistof met een hoeveelheid, δA, te vergroten, is dus een hoeveelheid arbeid, γ {\displaystyle \gamma } δA, nodig.  δA, nodig. Deze arbeid wordt opgeslagen als potentiële energie. Bijgevolg kan oppervlaktespanning in het SI-stelsel ook worden gemeten als joule per vierkante meter en in het cgs-stelsel als ergs per cm2 . Aangezien mechanische systemen een toestand van minimale potentiële energie proberen te vinden, neemt een vrije vloeistofdruppel van nature een bolvorm aan, die de minimale oppervlakte heeft voor een gegeven volume.
δA, nodig. Deze arbeid wordt opgeslagen als potentiële energie. Bijgevolg kan oppervlaktespanning in het SI-stelsel ook worden gemeten als joule per vierkante meter en in het cgs-stelsel als ergs per cm2 . Aangezien mechanische systemen een toestand van minimale potentiële energie proberen te vinden, neemt een vrije vloeistofdruppel van nature een bolvorm aan, die de minimale oppervlakte heeft voor een gegeven volume.
De gelijkwaardigheid van de meting van energie per oppervlakte-eenheid aan kracht per lengte-eenheid kan worden aangetoond door dimensionale analyse.
Oppervlakte kromming en druk
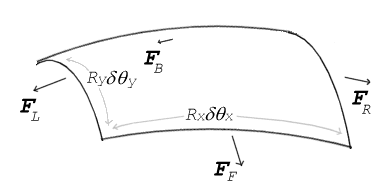
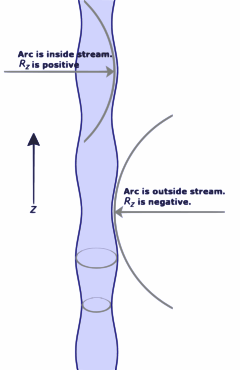
Als er geen kracht normaal op een gespannen oppervlak werkt, moet het oppervlak vlak blijven. Maar als de druk aan de ene kant van het oppervlak verschilt van de druk aan de andere kant, resulteert het drukverschil maal de oppervlakte in een normaalkracht. Om ervoor te zorgen dat de oppervlaktespanningskrachten de drukkracht opheffen, moet het oppervlak gekromd zijn. Het diagram toont hoe de kromming van een klein oppervlak leidt tot een netto component van oppervlaktespanningskrachten die normaal op het midden van het oppervlak werken. Wanneer alle krachten in evenwicht zijn, staat de resulterende vergelijking bekend als de vergelijking van Young-Laplace:
Δ p = γ ( 1 R x + 1 R y ) {displaystyle \Delta p = γ gamma \left({frac {1}{R_{x}}+{frac {1}{R_{y}}}right)}. 
waar:
· Δp is het drukverschil.
·  is de oppervlaktespanning.
is de oppervlaktespanning.
· Rx en Ry zijn kromtestralen in elk van de assen die evenwijdig zijn aan het oppervlak.
De grootheid tussen haakjes aan de rechterkant is in feite (tweemaal) de gemiddelde kromming van het oppervlak (afhankelijk van de normalisatie).
Oplossingen van deze vergelijking bepalen de vorm van waterdruppels, plassen, menisci, zeepbellen en alle andere vormen die door oppervlaktespanning worden bepaald. (Een ander voorbeeld is de vorm van de indrukken die de voeten van een schaatser maken op het oppervlak van een vijver).
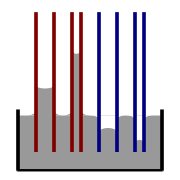
Onderstaande tabel laat zien hoe de interne druk van een waterdruppel toeneemt met afnemende straal. Voor niet al te kleine druppels is het effect subtiel, maar het drukverschil wordt enorm wanneer de druppels de moleculaire grootte benaderen. (In de limiet van een enkel molecuul wordt het begrip zinloos).
| Δp voor waterdruppels met verschillende stralen bij STP |
| Druppelstraal | 1 mm | 0,1 mm | 1 μm | 10 nm |
| Δp (atm) | 0.0014 | 0.0144 | 1.436 | 143.6 |
Vloeibaar oppervlak
Het is moeilijk om de vorm van het minimale oppervlak dat begrensd wordt door een willekeurig gevormd kader te vinden met alleen wiskunde. Maar door het frame te maken van draad en het in een zeepoplossing te dompelen, verschijnt er binnen enkele seconden een lokaal minimaal oppervlak in de resulterende zeeplaag.
De reden hiervoor is dat het drukverschil over een vloeistofinterface evenredig is met de gemiddelde kromming, zoals blijkt uit de vergelijking van Young-Laplace. Voor een open zeepfilm is het drukverschil nul, dus de gemiddelde kromming is nul, en minimale oppervlakken hebben de eigenschap van een gemiddelde kromming van nul.
Contacthoeken
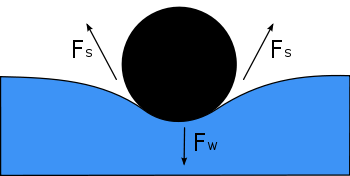
Het oppervlak van een vloeistof is een interface tussen die vloeistof en een ander medium. De bovenkant van een vijver is bijvoorbeeld een interface tussen het vijverwater en de lucht. Oppervlaktespanning is dus geen eigenschap van de vloeistof alleen, maar een eigenschap van het raakvlak van de vloeistof met een ander medium. Als een vloeistof zich in een vat bevindt, is er naast het raakvlak tussen vloeistof en lucht aan het bovenoppervlak ook een raakvlak tussen de vloeistof en de wanden van het vat. De oppervlaktespanning tussen de vloeistof en de lucht is meestal anders (groter) dan de oppervlaktespanning met de wanden van een vat. Waar de twee oppervlakken elkaar raken, zal de geometrie alle krachten in evenwicht houden.
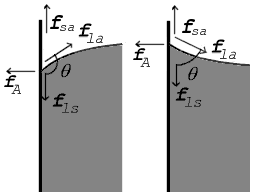
Waar de twee oppervlakken elkaar ontmoeten, vormen ze een contacthoek, θ {\scriptstyle \theta}.  Dit is de hoek die de raaklijn aan het oppervlak maakt met het vaste oppervlak. Het diagram rechts toont twee voorbeelden. De trekkrachten zijn weergegeven voor het grensvlak vloeistof-lucht, het grensvlak vloeistof-vaste stof en het grensvlak vaste stof-lucht. In het linker voorbeeld is het verschil tussen de oppervlaktespanning vloeistof-vaste stof en vaste stof-lucht, γ l s - γ s a {\displaystyle \scriptstyle \gamma _{mathrm {ls} }- gamma _{mathrm {sa} }}
Dit is de hoek die de raaklijn aan het oppervlak maakt met het vaste oppervlak. Het diagram rechts toont twee voorbeelden. De trekkrachten zijn weergegeven voor het grensvlak vloeistof-lucht, het grensvlak vloeistof-vaste stof en het grensvlak vaste stof-lucht. In het linker voorbeeld is het verschil tussen de oppervlaktespanning vloeistof-vaste stof en vaste stof-lucht, γ l s - γ s a {\displaystyle \scriptstyle \gamma _{mathrm {ls} }- gamma _{mathrm {sa} }}  is kleiner dan de oppervlaktespanning van de vloeistof in de lucht, γ l a {{\scriptstyle \gamma _{\mathrm {la}} }}
is kleiner dan de oppervlaktespanning van de vloeistof in de lucht, γ l a {{\scriptstyle \gamma _{\mathrm {la}} }}  maar is nog steeds positief, dat wil zeggen
maar is nog steeds positief, dat wil zeggen
γ l a > γ l s - γ s a > 0 {\displaystyle \gamma _{mathrm {la} }- gamma _{mathrm {ls}} }- gamma _{mathrm {sa} }\ >\ 0} 
In het diagram moeten zowel de verticale als de horizontale krachten precies opheffen in het contactpunt, het zogenaamde evenwicht. De horizontale component van f l a {\displaystyle \scriptstyle f_{\mathrm {la}}  wordt opgeheven door de kleefkracht, f A. }}
wordt opgeheven door de kleefkracht, f A. }}  .
.
f A = f l a sin θ {{{\mathrm {A}] = f_{mathrm {la}} sin \theta} 
Het belangrijkste krachtenevenwicht ligt echter in de verticale richting. De verticale component van f l a moet de kracht f l s precies opheffen.  moet de kracht f l s precies opheffen. }}
moet de kracht f l s precies opheffen. }}  .
.
f l s - f s a = - f l a cos θ {f_{mathrm {ls}} }-f_{mathrm {sa} = -f_{mathrm {la}} cos ^theta} 
| Vloeistof | Massief | Contacthoek |
| water | | soda lime glas | | loodglas | | gesmolten kwarts | | 0° |
| ethanol |
| diethylether |
| koolstoftetrachloride |
| glycerol |
| azijnzuur |
| water | paraffine | 107° |
| zilver | 90° |
| methyljodide | soda lime glas | 29° |
| loodglas | 30° |
| gesmolten kwarts | 33° |
| kwik | soda lime glas | 140° |
| Enkele contacthoeken tussen vloeistof en vaste stof |
Aangezien de krachten in directe verhouding staan tot hun respectieve oppervlaktespanningen, hebben we ook:
γ l s - γ s a = - γ l a cos θ {\displaystyle \gamma {ls} }-\gamma _{mathrm {sa} = -gamma _{mathrm {la}} cos \theta} 
waarbij
· γ l s {{{\scriptstyle \gamma}} }} is de vloeistof-vaste stof oppervlaktespanning,
is de vloeistof-vaste stof oppervlaktespanning,
· γ l a {{{\scriptstyle \gamma}}. }} is de vloeistof-lucht oppervlaktespanning,
is de vloeistof-lucht oppervlaktespanning,
· γ s a {{{\scriptstyle \gamma}}. }} is de oppervlaktespanning tussen vaste stof en lucht,
is de oppervlaktespanning tussen vaste stof en lucht,
·  is de contacthoek, waarbij een concave meniscus een contacthoek van minder dan 90° heeft en een convexe meniscus een contacthoek van meer dan 90°.
is de contacthoek, waarbij een concave meniscus een contacthoek van minder dan 90° heeft en een convexe meniscus een contacthoek van meer dan 90°.
Dit betekent dat hoewel het verschil tussen de vloeistof-vaste stof en vaste stof-lucht oppervlaktespanning, γ l s - γ s a {\displaystyle \scriptstyle \gamma _{mathrm {ls} }- gamma _{mathrm {sa} }}  is moeilijk rechtstreeks te meten, maar kan worden afgeleid uit de oppervlaktespanning tussen vloeistof en lucht, γ l a {{\displaystyle \mathrm {la}} }}
is moeilijk rechtstreeks te meten, maar kan worden afgeleid uit de oppervlaktespanning tussen vloeistof en lucht, γ l a {{\displaystyle \mathrm {la}} }}  en de evenwichtscontacthoek, θ {\displaystyle \scriptstyle \theta}.
en de evenwichtscontacthoek, θ {\displaystyle \scriptstyle \theta}.  die een functie is van de gemakkelijk meetbare in- en uitgaande contacthoek (zie hoofdartikel contacthoek).
die een functie is van de gemakkelijk meetbare in- en uitgaande contacthoek (zie hoofdartikel contacthoek).
Dit verband bestaat ook in het diagram rechts. Maar in dit geval zien we dat, omdat de contacthoek kleiner is dan 90°, het verschil in oppervlaktespanning tussen vloeistof en vaste stof/lucht negatief moet zijn:
γ l a > 0 > γ l s - γ s a {\displaystyle \gamma _{mathrm {la}} γgamma _{mathrm {ls}} }- gamma _{mathrm {sa} }} 
Speciale contacthoeken
Merk op dat in het speciale geval van een water-zilver interface waar de contacthoek gelijk is aan 90°, het verschil in oppervlaktespanning tussen vloeistof en vaste stof/lucht precies nul is.
Een ander speciaal geval is wanneer de contacthoek precies 180° is. Water met speciaal geprepareerd Teflon benadert dit. Een contacthoek van 180° ontstaat wanneer de vloeistof-vaste stof oppervlaktespanning precies gelijk is aan de vloeistof-lucht oppervlaktespanning.
γ l a = γ l s - γ s a > 0 θ = 180 ∘ {\gamma _{mathrm {la}} = gamma _{mathrm {ls}} }- gamma _{mathrm {sa} 0 Kwadraat \theta \ = 180^{circ}}. 















































.jpg)