Thermodynamica
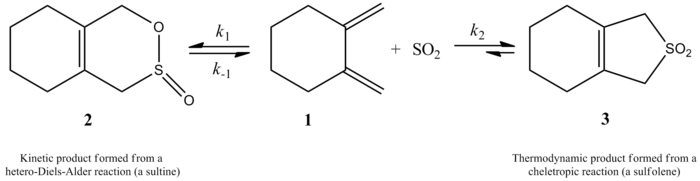
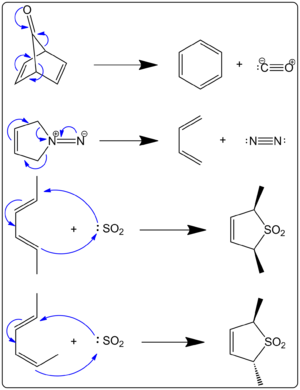
Wanneer zwaveldioxide reageert met butadieen en isopreen, ontstaan er twee verschillende producten. Het reactiemechanisme bepaalt wat er gemaakt wordt. Een kinetisch product en een thermodynamisch product zijn beide mogelijk. Van het thermodynamische product wordt meer gemaakt dan van het kinetische product. Het kinetische product komt voort uit een Diels-Alderreactie, terwijl een cheletropische reactie een thermodynamisch stabieler product maakt. De cheletropische route wordt meer gebruikt omdat deze tot een stabieler adduct met vijf ringen leidt. Het onderstaande schema toont het verschil tussen de twee producten. Het pad links toont het thermodynamische product, terwijl het pad rechts het kinetische product toont. Suarez en Sordo toonden dit aan in 1995. Zij toonden dit zowel met experimenten als met Gaussiaanse berekeningen aan.
Kinetiek
Een voorbeeld hiervan zijn de cheletropische reacties van 1,3-dieen met zwaveldioxide. Chemici hebben zorgvuldig gekeken naar de kinetiek van deze reactie. In 1976 maten Isaacs en Laila de kenetische factoren voor de toevoeging van zwaveldioxide aan butadieenderivaten. De toevoegingssnelheid werd gecontroleerd in benzeen bij 30 °C met een aanvankelijke twintigvoudige overmaat aan diene. Zij gebruikten een spectrofotometer om het licht bij 320 nm te bestuderen om het verdwijnen van SO2 te meten. De reactie vertoonde een "pseudo-eerste-orde-kinetiek". De chemici ontdekten dat elektronenonttrekkende groepen op het diene de reactiesnelheid verminderden. Ook werd de reactiesnelheid aanzienlijk beïnvloed door sterische effecten van 2-substituenten, waarbij meer volumineuze groepen de reactiesnelheid verhoogden. (Met andere woorden, hoe groter de groep atomen die aan het tweede koolstofatoom hangt, hoe sneller de reactie verloopt). De auteurs schrijven dit toe aan de neiging van volumineuze groepen om de cisoïde conformatie van het diene te bevorderen, die essentieel is voor de reactie (zie onderstaande tabel). Bovendien werden de snelheden bij vier temperaturen gemeten voor zeven van de diënen. Op basis van deze metingen gebruikten chemici de Arrheniusvergelijking om voor elke reactie de enthalpie van activering (ΔH‡ ) en de entropie van activering (ΔS‡ ) te berekenen. Dit was een van de eerste belangrijke pogingen om de kenetiek van een cheletropische reactie te bestuderen.
| -Butadieen | 104 k /min−1 (30 °C) (± 1-2%) absoluut | 104 k /min−1 (30 °C) (± 1-2%) relatief | ΔH‡ /kcal mol−1 | ΔS‡ /cal mol−1 K−1 |
| 2-methyl | 1.83 | 1.00 | 14.9 | -15 |
| 2-ethyl | 4.76 | 2.60 | 10.6 | -20 |
| 2-isopropyl | 13.0 | 7.38 | 12.5 | -17 |
| 2-tert-butyl | 38.2 | 20.8 | 10.0 | -19 |
| 2-neopentyl | 17.2 | 9.4 | 11.6 | -18 |
| 2-cloro | 0.24 | 0.13 | N.V.T. | N.V.T. |
| 2-broomethyl | 0.72 | 0.39 | N.V.T. | N.V.T. |
| 2-p-tolyl | 24.7 | 13.5 | 10.4 | -19 |
| 2-fenyl | 17.3 | 9.45 | N.V.T. | N.V.T. |
| 2-(p-broomfenyl) | 9.07 | 4.96 | N.V.T. | N.V.T. |
| 2,3-dimethyl | 3.54 | 1.93 | 12.3 | -18 |
| cis-1-methyl | 0.18 | 0.10 | N.V.T. | N.V.T. |
| trans-1-methyl | 0.69 | 0.38 | N.V.T. | N.V.T. |
| 1,2-dimethyleen-cyclohexaan | 24.7 | 13.5 | 11.4 | -16 |
| 2-methyl-1,1,4,4-d4 | 1.96 | N.V.T. | N.V.T. | N.V.T. |
Monnat, Vogel en Sordo hebben in 2002 de kinetiek gemeten van de toevoeging van zwaveldioxide aan 1,2-dimethylidenecycloalkanen. Zij schreven dat de reactie van 1,2-dimethylidenecyclohexaan met zwaveldioxide twee verschillende producten kan opleveren, afhankelijk van de reactieomstandigheden. De reactie maakt het overeenkomstige sultine via een hetero-Diels-Alder reactie onder kinetische controle (≤ -60 °C), maar onder thermodynamische controle (≥ -40 °C) maakt de reactie het overeenkomstige sulfoleen via een cheletropische reactie. De activeringsenthalpie voor de hetero-Diels-Alder reactie is ongeveer 2 kcal/mol kleiner dan die voor de overeenkomstige cheletropische reactie. Het sulfoleen is ongeveer 10 kcal/mol stabieler dan het isometrische sultine in CH2 Cl2 /SO2 oplossing.
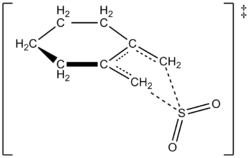
De auteurs konden experimenteel een snelheidswet uitwerken bij 261,2 K voor de reactie van 1,2-dimethylidenecyclohexaan met zwaveldioxide tot het overeenkomstige sulfoleen. De reactie was eerste orde in 1,2-dimethylidenecyclohexaan, maar tweede orde in zwaveldioxide (zie hieronder). Dit bevestigde een voorspelling van theoretische chemici op basis van hoogwaardige ab initio kwantumberekeningen. Met behulp van computationele methoden hebben de auteurs een overgangsstructuur voorgesteld voor de cheletropische reactie van 1,2-dimethylidenecyclohexaan met zwaveldioxide (zie figuur rechts). De reactie is tweede orde in zwaveldioxide omdat een andere zwaveldioxidemolecuul zich waarschijnlijk bindt aan de overgangstoestand om deze te helpen stabiliseren. Vergelijkbare resultaten werden gevonden in een studie uit 1995 van Suarez, Sordo en Sordo, die ab initio berekeningen gebruikten om de kinetische en thermodynamische controle van de reactie van zwaveldioxide met 1,3-dieen te bestuderen.
d [ 3 ] d t = k 2 [ 1 ] [ S O 2 ] 2 {{displaystyle {frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}} ![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)
Effecten van oplosmiddelen
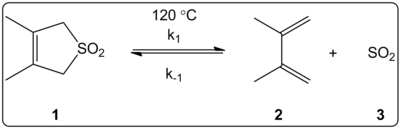
Het effect van het oplosmiddel van de cheletropische reactie van 3,4-dimethyl-2,5-dihydrothiofeen-1,1-dioxide (rechts getoond) werd kinetisch onderzocht in 14 oplosmiddelen. De reactiesnelheidsconstanten van de voorwaartse en omgekeerde reactie en de evenwichtsconstanten bleken lineair gecorreleerd met de ET (30) polariteitsschaal van het oplosmiddel.
De reacties vonden plaats bij 120 °C en werden bestudeerd met 1H-NMR-spectroscopie van het reactiemengsel. De voorwaartse snelheid k1 bleek met een factor 4,5 af te nemen van cyclohexaan naar methanol. De omgekeerde snelheid k-1 bleek met een factor 53 toe te nemen bij de overgang van cyclohexaan naar methanol, terwijl de evenwichtsconstante Keq met een factor 140 afnam. Er wordt gesuggereerd dat de polariteit tijdens het activeringsproces verandert, zoals blijkt uit de relaties tussen de evenwichts- en kinetische gegevens. De auteurs zeggen dat de reactie lijkt te worden beïnvloed door de polariteit van het oplosmiddel, en dit kan worden aangetoond door de verandering in de dipoolmomenten bij de overgang van reactant naar overgangstoestand naar product. De auteurs stellen ook dat de cheletropische reactie niet lijkt te worden beïnvloed door de zuurgraad of basiciteit van het oplosmiddel.
De resultaten van deze studie doen de auteurs de volgende gedragingen verwachten:
1. De verandering in de polariteit van het oplosmiddel zal de snelheid minder beïnvloeden dan het evenwicht.
2. De snelheidsconstanten worden gekenmerkt door een tegengesteld effect op de polariteit: k1 zal licht afnemen met de toename van ET (30), en k-1 zal toenemen onder dezelfde omstandigheden.
3. Het effect op k-1 zal groter zijn dan op k1 .

![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)