V: Wat is een aromatische koolwaterstof?
A: Een aromatische koolwaterstof is een koolwaterstofringverbinding met afwisselend dubbele en enkele bindingen tussen koolstofatomen die ringen vormen, en veel van deze verbindingen hebben een zoete geur.
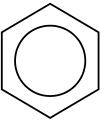
V: Wat is de naam van de ring van zes koolstofatomen in aromatische verbindingen?
A: De naam van de ring van zes koolstofatomen in aromatische verbindingen is een benzeenring.
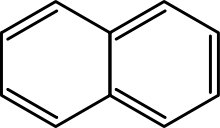
V: Wat is het verschil tussen monocyclische (MAH) en polycyclische (PAK) aromatische koolwaterstoffen?
A: Monocyclische aromatische koolwaterstoffen (MAH) hebben een enkele ring van koolstofatomen in hun structuur, terwijl polycyclische aromatische koolwaterstoffen (PAK) twee of meer verbonden ringen van koolstofatomen in hun structuur hebben.
V: Waarom worden aromatische koolwaterstoffen "aromatisch" genoemd?
A: Aromatische koolwaterstoffen worden "aromatisch" genoemd omdat veel ervan een zoete geur hebben.
V: Wat zijn heterogenen en waarin verschillen ze van aromatische verbindingen op basis van benzeen?
A: Heteroarenen zijn verbindingen zonder benzeen die de regel van Hückel volgen en die ook aromatische verbindingen zijn. In deze verbindingen is minstens één koolstofatoom vervangen door één van zuurstof, stikstof of zwavel.
V: Wat is de eenvoudigst mogelijke koolwaterstofring?
A: De eenvoudigst mogelijke koolwaterstofring is benzeen.
V: Wat zijn de twee soorten aromatische koolwaterstoffen?
A: De twee soorten aromatische koolwaterstoffen zijn monocyclische (MAH) en polycyclische (PAH) aromatische koolwaterstoffen.