Directed evolution (DE) is een experimentele methode om enzymen en andere eiwitten zodanig te verbeteren of te wijzigen dat ze beter voldoen aan industriële, medische of biotechnologische eisen. In plaats van te vertrouwen op gedetailleerde structurele kennis van een eiwit, benut DE herhaalde rondes van variatie en selectie om eigenschappen zoals hogere activiteit, verhoogde thermostabiliteit, veranderde specificiteit of verminderde toxiciteit te bereiken.
Basisprincipe
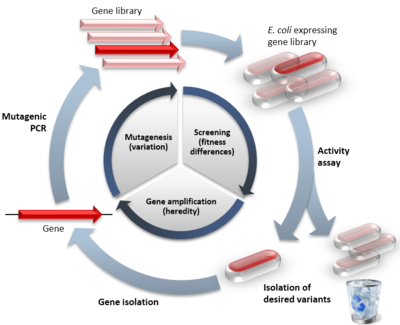
DE is een vorm van proteïnetechniek die de natuurlijke selectie nabootst. Het doorgaande patroon is:
- genereren van variatie in een start-gen (mutaties of recombinatie),
- produceren van een bibliotheek van verschillende eiwitvarianten,
- testen of selecteren van varianten met de gewenste eigenschap,
- gebruik van de beste varianten als sjabloon voor volgende rondes.
Concreet laat men een gen door herhaalde ronden van mutatie lopen om een diversiteit aan varianten te maken. Vervolgens worden genen met de gewenste functie geïsoleerd en gebruikt als sjabloon voor de volgende ronde, waardoor cumulatieve verbetering mogelijk wordt.
Methoden om variatie te creëren
Veelgebruikte technieken om diversiteit te genereren zijn onder andere:
- error-prone PCR (verhoogde foutfrequentie tijdens amplificatie),
- DNA-shuffling of recombinatie tussen verwante genen,
- site-saturation mutagenese (gericht variëren op geselecteerde aminozuurposities),
- gebruik van mutator strains of chemische mutagenen,
- combinaties van bovengenoemde methoden om zowel lokale als grootschalige veranderingen te verkrijgen.
In vivo versus in vitro uitvoering
DE kan zowel in vivo als in vitro worden uitgevoerd. Bij in vivo experimenten wordt elke cel (meestal bacteriën of gist) getransformeerd met een plasmide dat een andere varianten uit de bibliotheek bevat. Alleen het betrokken gen varieert tussen cellen; alle andere genetische achtergrond blijft meestal hetzelfde. De cellen drukken het eiwit uit in hun cytoplasma of op hun oppervlak, zodat de functie kan worden getest binnen een cellulaire context. Dit is nuttig wanneer het geëvolueerde eiwit of RNA later in levende organismen moet functioneren.
Bij in vitro DE wordt gebruikgemaakt van vrije transcriptievertaling om eiwitten of RNA in oplossing of binnen kunstmatige microdruppels te produceren. Dit biedt voordelen zoals controle over omstandigheden (temperatuur, oplosmiddelen), expressie van eiwitten die toxisch zouden zijn voor cellen, en de mogelijkheid om extreem grote bibliotheken te onderzoeken (tot 1015) omdat het bibliotheek-DNA niet in cellen hoeft te worden ingebracht. Dat laatste is vaak een beperkende stap bij in vivo-methoden.
Selectie en screening
Een essentieel verschil is selectie versus screening:
- Selectie: alleen cellen of moleculen met de gewenste eigenschap overleven of worden waargenomen (efficiënt voor zeer grote bibliotheken).
- Screening: elke variant wordt afzonderlijk getest en beoordeeld (meer arbeidsintensief maar flexibeler voor complexe eigenschappen).
High-throughput methoden zoals FACS, microfluidische droplet-assays en automatisering maken het mogelijk om miljoenen varianten snel te analyseren en de beste kandidaten te isoleren.
Toepassingen
Directed evolution wordt breed toegepast, onder meer voor:
- verbeteren van industriële enzymen (bijv. hogere stabiliteit, bredere pH- of temperatuurbereiken),
- ontwikkelen van biokatalysatoren voor synthese van medicijnen en fijnchemicaliën,
- creëren van enzymen met gewijzigde of verbeterde substraatselectiviteit of enantioselectiviteit,
- verbeteren van therapeutische eiwitten en antilichamen,
- ontwerpen van biosensoren en nieuwe functionaliteiten voor synthetische biologie.
Voordelen en beperkingen
Voordelen:
- werkt vaak zonder gedetailleerde structurele informatie van het eiwit,
- kan eigenschappen vinden die moeilijk te voorspellen zijn met computationele modellen,
- flexibel: toepasbaar op enzymen, RNA, bindingsdomeinen en hele pathways.
Beperkingen en uitdagingen:
- vereist een betrouwbare selectie- of screeningassay die correleert met de gewenste functie,
- kan vastlopen in lokale optima; combinatorische complexiteit vereist slimme bibliotheekontwerpen,
- ethische en veiligheidsaspecten bij werken met gemodificeerde organismen of bioactieve eiwitten,
- soms trade-offs: verbetering in één eigenschap kan andere eigenschappen nadelig beïnvloeden.
Geschiedenis en opvattingen
Directed evolution is ontwikkeld en populair gemaakt door onderzoekers die methoden combineerden voor mutatie en selectie op laboratoriumschaal. Een van de bekendste pioniers is Frances Arnold, die aanzienlijke bijdragen leverde aan het veld en hiervoor erkenning kreeg. Het succes van DE illustreert hoe laboratoriumversies van evolutionaire principes krachtige oplossingen kunnen opleveren voor technische en medische vragen.
Veiligheid en ethiek
Bij DE-experimenten moeten standaard laboratoriumveiligheidsprocedures gelden, inclusief passende biocontainment en risicobeoordelingen, vooral wanneer geëvolueerde eiwitten nieuwe biologische activiteiten hebben. Regulering en verantwoord gebruik zijn belangrijk om dual-use-risico’s te minimaliseren en om maatschappelijke en milieu-overwegingen mee te nemen.
Samengevat is directed evolution een robuuste en veelzijdige strategie om eiwitten en enzymen te optimaliseren. Door herhaalde variatie en gerichte selectie kunnen eigenschappen worden verbeterd die moeilijk te bereiken zijn met puur rationeel ontwerp, waardoor DE een kerntechnologie is geworden in moderne biotechnologie en synthetische biologie.