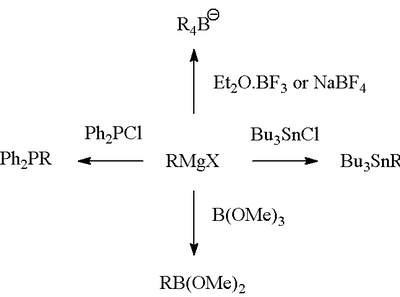
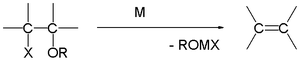
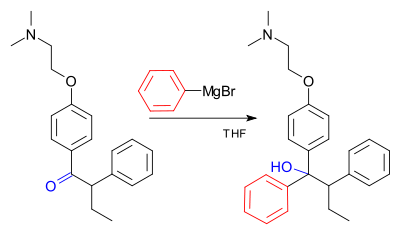
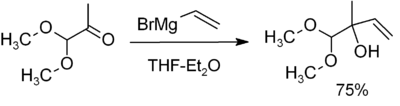De Grignardreactie (uitgesproken als /ɡriɲar/) is een fundamentele organometaalchemische reactie waarbij alkyl- of aryl-magnesiumhalogeniden (Grignardreagentia, algemeen aangeduid als RMgX) elektrofiele koolstofatomen aanvallen die aanwezig zijn in sterk gepolariseerde bindingen, bijvoorbeeld in carbonylgroepen. Grignard-reagentia gedragen zich als sterke nucleofielen en basen en worden in de organische synthese veel gebruikt om nieuwe koolstof–koolstofverbindingen te vormen. De reactie verandert de hybridisatie van het reactiecentrum (bijvoorbeeld sp2 naar sp3 bij additie op een carbonyl) en kan ook leiden tot bindingen tussen koolstof en heteroatomen zoals P, Sn, Si en B.
Structuur en aggregatie
Een Grignard-reagens wordt niet als vrije carbanion geïsoleerd maar komt voor als een geaggregeerde organometaalkluster, meestal gecoördineerd door etheroplosmiddelen (bijv. di-ethylether of THF). In oplossing bestaat vaak een evenwicht tussen verschillende complexen (het zogenaamde Schlenk-evenwicht) waarbij RMgX, R2Mg en MgX2 in verschillende verhoudingen kunnen voorkomen. De coördinatie van het oplosmiddel aan magnesium stabiliseert het reagent en beïnvloedt zijn reactiviteit.
Bereiding en reactionele voorwaarden
Een typisch bereidingsschema van een Grignard-reagens is de reactie van een alkyl- of arylhalogenide met magnesiummetaal in droge, zuurstofvrije etherische oplosmiddelen:
- Oplosmiddelen: droge di-ethylether of tetrahydrofuraan (THF) zijn gebruikelijk omdat zij goed coördineren aan Mg en het reagent stabiliseren.
- Droogte en inert atmosphere: Grignard-reagentia reageren heftig met protische stoffen (H2O, alcoholen, aminen) en met zuurstof. Daarom wordt gewerkt onder droge inertgasatmosfeer (N2 of Ar) en met vlamgedroogd glaswerk of Schlenk-techniek.
- Activatie van magnesium: het oppervlak van magnesium kan geoxideerd zijn. Methoden om het actief te maken zijn mechanische reiniging, toevoeging van een kleine hoeveelheid jodium of 1,2-dibroomethaan, of gebruik van ultrasoon/‘sonificatie’ of ‘Rieke Mg’-methoden.
Mechanisme (basisstappen)
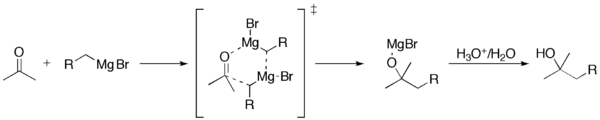
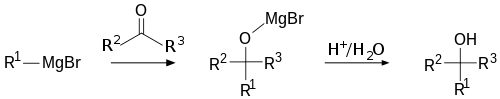
Het algemene mechanisme voor een additie op een carbonylverbinding omvat de volgende stappen:
- Vorming van het Grignard-reagens: R–X + Mg → RMgX (initiëren via electron-overdracht en vorming van organometaalklusters).
- Nucleofiele additie: het carbanion-achtige R^–-deel van RMgX valt het elektrofiele koolstofatoom van de carbonylgroep aan, waardoor een tetraëdrische alkoxide-magnesiumberbinding ontstaat.
- Zuiverings-/werk-upstap: na toevoeging van een protonbron (zuur of water) wordt het alkoxide geprotoneerd en ontstaat het corresponderende alcohol (bijvoorbeeld primaire, secundaire of tertiaire alcohol afhankelijk van de beginmaterialen).
Voorbeeld: additie van een Grignard-reagens aan een aldehyde of keton geeft na zure werk-up een alcohol. Additie aan CO2 levert na zure werk-up een carboxylaat (daarna protonatie tot een carbonzuur).
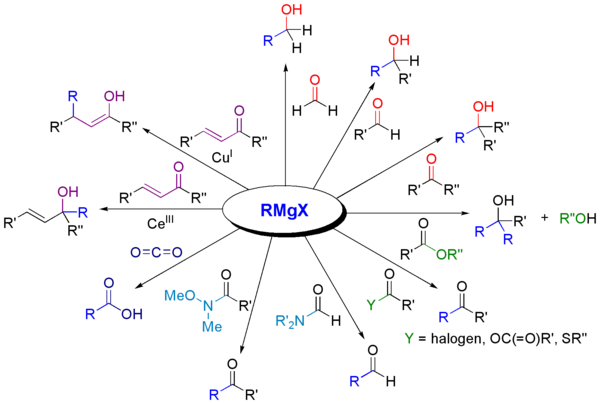
Reikwijdte en typische reacties
- Additie aan carbonylverbindingen: primair, secundair en tertair alcohol (afhankelijk van carbonyl- en Grignard-substituenten).
- Carboxylatie: opname van CO2 gevolgd door zure werk-up geeft carboxylzuren.
- Reacties met esters: esters reageren doorgaans twee keer met een Grignard-reagens; na dubbele additie en hydrolyse ontstaat een tertiair alcohol (indien het reagens twee equivalents levert).
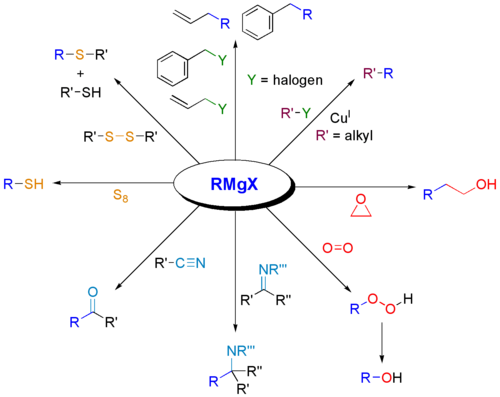
- Halogen–metaaluitwisseling: RMgX kan halogenen verwisselen met andere organohalogeniden onder geschikte voorwaarden.
- Conjugaataddities en cross-couplings: directe 1,2- versus 1,4-additie is afhankelijk van substraten en zouten; voor selectieve 1,4-additie worden vaak gemodificeerde reagentia of katalysatoren (CuI → Gilman-achtige reagentia) gebruikt.
Beperkingen en nevenreacties
- Grignard-reagentia zijn zeer gevoelig voor protische functionele groepen (–OH, –NH, –COOH), dus substraten moeten vrij zijn van dergelijke groepen of vooraf geblokkeerd worden.
- Contact met water of lucht verlaagt het rendement doordat het reagent geprotoneerd wordt en onwerkzaam raakt.
- Sterk gehinderde of bepaalde functionele groepen kunnen de vorming van RMgX of de gewenste additie verhinderen.
- Directe reactie tussen een Grignard-reagens en een alkylhalogenide om C–C-bindingen te vormen via een SN2-mechanisme is vaak niet effectief; in plaats daarvan treden bij de vormingsstap enkel-electronoverdracht-processen op die radicalaire bijproducten of koppelingen (bijv. Wurtz-type) kunnen geven. Daarom worden voor substituties vaak alternatieve routes (bijv. organolithium, organozink of gekatalyseerde cross-coupling zoals Suzuki, Negishi) gebruikt.
Praktische tips en veiligheidsaspecten
- Werk onder inert gas en met droog glaswerk; vlamdrogen is een vaak gebruikte techniek om vocht te verwijderen.
- Magnesiumreacties kunnen sterk exotherm verlopen; portionering van reagentia en temperatuurregeling zijn belangrijk.
- Ultrageluid of toevoeging van activatoren (zoals jodium of 1,2-dibroomethaan) kan de initiatie van de Grignardvorming vergemakkelijken.
- Grignardreagentia zijn brandbaar en reageren met zuren; draag geschikte persoonlijke beschermingsmiddelen en zorg voor goede ventilatie.
Varianten en alternatieven
Er bestaan veel aanpassingen en alternatieven voor klassieke Grignard-reagentia, waaronder organolithiumverbindingen (nog sterker nucleofiel en base), Gilman-reagentia (organocupraten voor selectieve cross-coupling en conjugaataddities), en organozink- of -boronverbindingen (milder en toleranter voor functionele groepen). Voor moeilijk te vormen Grignard-reagentia kan men gebruikmaken van “Rieke”-metalen of katalytische transmetalatieprocedés.
De Grignardreactie is genoemd naar François Auguste Victor Grignard, de Franse scheikundige van de Universiteit van Nancy, die voor zijn onderzoek naar deze organometaalverbindingen in 1912 de Nobelprijs voor scheikunde ontving.