De SN1-reactie is een substitutiereactie in de organische chemie. "SN" staat voor nucleofiele substitutie en de "1" staat voor het feit dat bij de snelheidsbepalende stap slechts één molecuul betrokken is (unimoleculair). Bij de reactie is een carbokation-tussenproduct betrokken. Enkele veel voorkomende SN1-reacties zijn van secundaire of tertiaire alkylhalogeniden onder sterk basische omstandigheden of, onder sterk zure omstandigheden, met secundaire of tertiaire alcoholen. Met primaire alkylhalogeniden treedt de alternatieve SN2-reactie op. Onder anorganische scheikundigen staat de SN1-reactie vaak bekend als het dissociatieve mechanisme. Christopher Ingold et al. stelden het reactiemechanisme voor het eerst voor in 1940.
Mechanisme
De typische SN1-reactie verloopt via twee hoofdstappen:
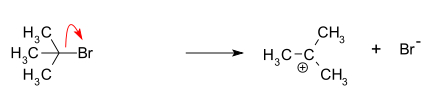
- Stap 1 (snelheidsbepalend): heterolytische afsplitsing van de leaving group (LG) van het substraat R–LG, waardoor een carbokation (R+) en de leaving group anion (LG–) ontstaan. Deze stap is unimoleculair en bepaalt de reactiesnelheid.
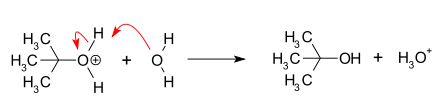
- Stap 2: het gevormde carbokation wordt door een nucleofiel (Nu) aangevallen, waardoor het substitutieproduct R–Nu ontstaat.
Samengevat: R–LG → R+ + LG– (traag), gevolgd door R+ + Nu → R–Nu (snel).
Kenmerken en kinetiek
- Reactiesnelheid: eerste-orde kinetiek: v = k [substraat]. De snelheid hangt alleen af van de concentratie van het uitgangsmolecuul (unimoleculair).
- Hammond-principe: bij endotherme ionisatie heeft de overgangstoestand veel carbokation-karakter; stabilisatie van het carbokation verlaagt de activeringsenergie en versnelt de reactie.
- Rol van het nucleofiel: een sterk nucleofiel versnelt SN2, maar bij SN1 speelt het nucleofiel in de snelheidsbepalende stap nauwelijks een rol; zwakkere nucleofielen zijn bij SN1 vaak voldoende.
Factoren die SN1 bevorderen
- Substraatstructuur: stabilisatie van het carbokation is cruciaal. Tertiaire > secundaire > primaire; stabiliserende substituenten (alkylgroepen, resonantie zoals bij benzyl- of allylcarbokationen) bevorderen SN1.
- Leaving group: goede leaving groups (bijv. I–, Br–, tosylaat, water na protonering) vergemakkelijken de ionisatie.
- Oplosmiddel: polar protische oplosmiddelen (water, alcoholen) solvaseren en stabiliseren zowel het carbokation als het leaving-group anion, en bevorderen SN1.
- Zuurgraad: protonering van alcoholen zet een slechte leaving group (OH) om in water, een goede leaving group, waardoor SN1 mogelijk wordt onder zure omstandigheden.
- Temperatuur en concurrerende processen: hogere temperatuur kan eliminatie (E1) bevorderen; bij afwezigheid van sterke nucleofielen of bij verwarmde omstandigheden is E1 vaak concurrerend.
Stereochemie en ion pairs
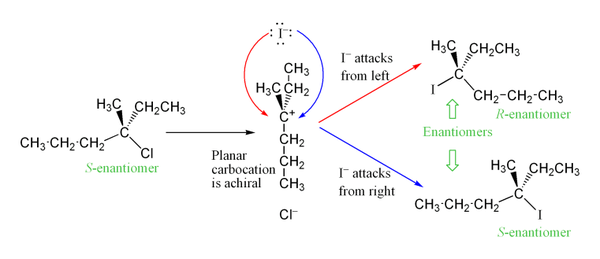
Het carbokation is plannair (sp2) en kan vanaf beide zijden aangevallen worden, wat vaak leidt tot racemisatie wanneer het uitgangsmateriaal chirale centra bevat. Volledige racemisatie wordt niet altijd bereikt: soms ontstaat een ion pair (intimate ion pair) waarbij het anion tijdelijk dicht bij het carbokation blijft en de aanval van het nucleofiel gedeeltelijk van één zijde voorkomt, wat leidt tot gedeeltelijke retentie of inversie.
Rearrangementen
Carbokationen kunnen ondergaan tot verschuivingen (hydride- of alkylverschuivingen) naar een meer gestabiliseerd carbokation. Dit verklaart waarom soms onverwachte producten optreden: het gevormde carbokation kan eerst herstructureren en daarna door een nucleofiel worden gevangen.
Voorbeelden
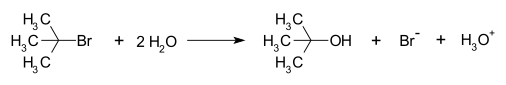
- Hydrolyse van tert-butylchloride in water: (CH3)3C–Cl + H2O → (CH3)3C–OH + HCl. Ionisatie geeft het tert-butylcarbokation dat door water wordt aangevallen.
- Solvolyse van 2-bromo-2-methylpropaan (tert-butylbromide) in ethanol geeft tert-butylethanol en bromide: (CH3)3C–Br + EtOH → (CH3)3C–OEt + HBr (via SN1 / solvolyse).
- Benzyl- en allylhalogeniden: ondanks dat ze primair kunnen zijn, geven ze SN1-achtige reacties door resonantiestabilisatie van het carbokation (bijv. benzylchloride → benzylalcohol in waterige omstandigheden).
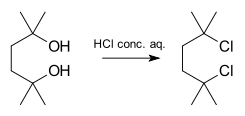
- Protonering van tertiaire alcoholen onder zure condities leidt tot vertrek van water en vorming van een tertiair carbokation dat door nucleofielen kan worden opgevangen.
Concurrentie met andere mechanismen
SN1 concurreert vaak met E1 (unimoleculaire eliminatie). Beide verlopen via hetzelfde carbokation tussenproduct; welke reactie dominant is hangt af van temperatuur, nucleofiel/basis, en concentraties. SN2 daarentegen is bimoleculair en wordt bevorderd door sterke nucleofielen, polaire aprotische oplosmiddelen en minder gehinderde (primaire) substraten.
Praktische overwegingen
- Bij synthetische toepassingen: kies een substraat en oplosmiddel die carbokationstabilisatie ondersteunen wanneer SN1 gewenst is (bijv. tertiaire halogeniden in water of alcoholen).
- Let op mogelijke rearrangementen die tot bijproducten kunnen leiden.
- Controleer of eliminatie (E1) ongewenst is; lagere temperatuur en aanwezigheid van nucleofiel kunnen SN1-producten bevorderen, maar soms is selectiviteit moeilijk te krijgen.
Samengevat: de SN1-reactie is een unimoleculair substitutiemechanisme via een carbokation tussenproduct. Het wordt vooral gefaciliteerd door stabiele carbokationen, goede leaving groups en polar protische oplosmiddelen. Begrip van factoren als stereochemie, rearrangementen en competitie met E1 is essentieel voor het voorspellen en sturen van het reactie-uitkomst in de praktijk.